
Olá, estimados profissionais de Regulamentação! Como membro da indústria das ciências da vida, é provável que esteja familiarizado com o formato de submissão do Documento Técnico Comum Eletrónico (eCTD) que está a revolucionar a indústria de Regulamentação das Ciências da Vida. A sua estrutura padronizada é uma verdadeira mudança de paradigma. Com este blog, pretendemos fornecer informações valiosas sobre as melhores práticas para submissões eCTD. Então, preparemo-nos para nos tornarmos especialistas em submissões eCTD juntos!
Submissões eCTD e Melhores Práticas
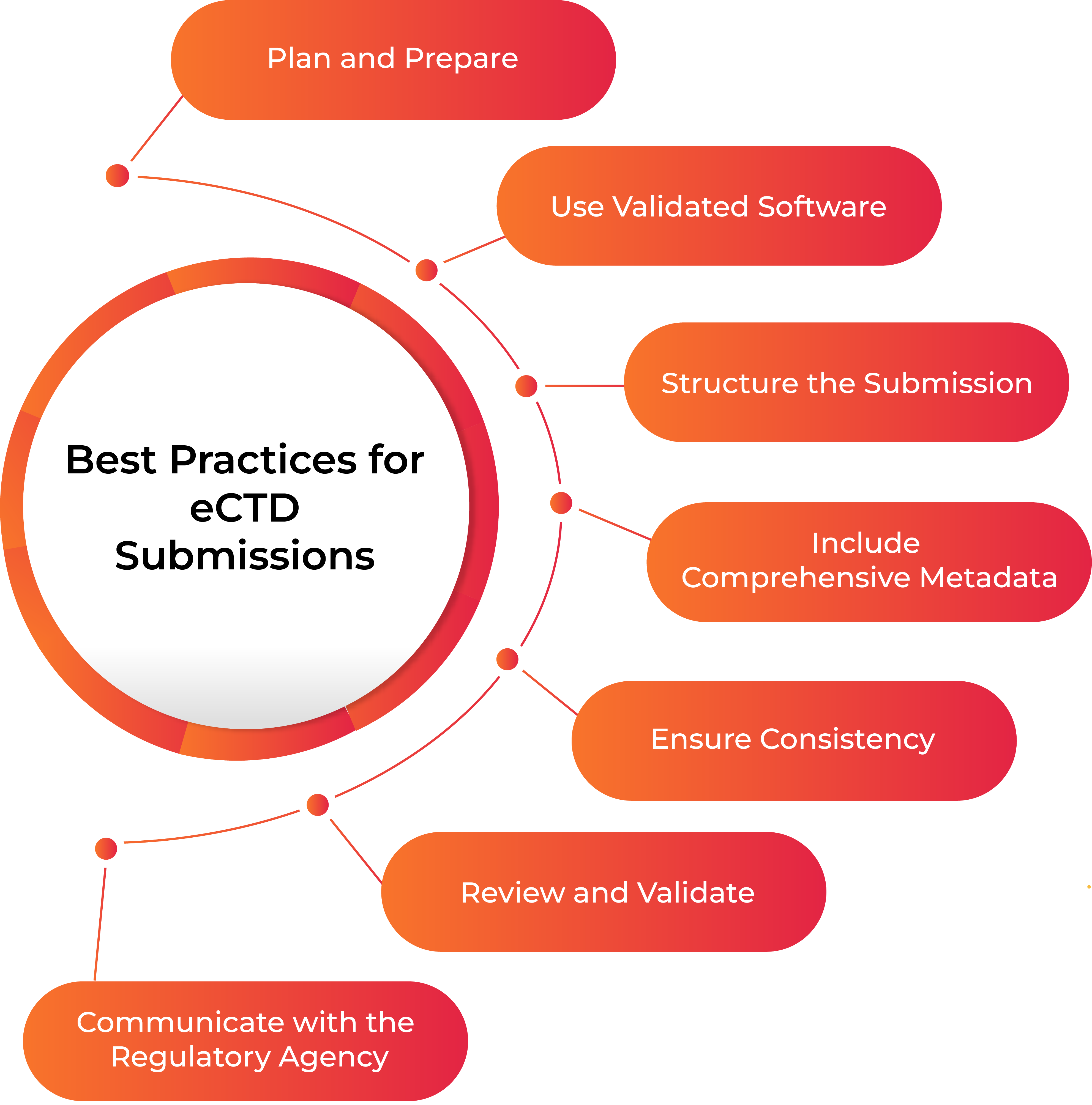
Para garantir uma submissão eCTD bem-sucedida, é essencial cumprir os requisitos regulamentares e seguir as melhores práticas, conforme ilustrado na imagem abaixo:
Planear e Preparar
Desenvolver um plano detalhado é o primeiro passo para uma submissão eCTD bem-sucedida. O plano deve incluir um cronograma, marcos e responsabilidades para cada membro da equipa envolvido no processo de submissão. Deve ser alocado tempo adequado para a revisão e aprovação do pacote de submissão. Todos os documentos necessários devem ser preparados e organizados de acordo com as diretrizes regulamentares aplicáveis.
Utilize Software Validado
O software de submissão eCTD deve ser validado para garantir que cumpre os requisitos regulamentares. O software deve ser capaz de gerar submissões eCTD sem erros e bem estruturadas. Além disso, o software deve ser frequentemente atualizado para se alinhar com os mais recentes requisitos regulamentares.
Estruturar a Submissão
Uma submissão eCTD bem estruturada facilita uma revisão regulamentar eficiente. A submissão deve ser estruturada de acordo com as especificações eCTD do Conselho Internacional para a Harmonização (ICH) e as especificações regionais do Módulo 1. Cada submissão deve ter uma estrutura de pastas claramente definida e consistente em todo o pacote de submissão.
Incluir Metadata Abrangente
Metadata fornece informações adicionais sobre os documentos no pacote de submissão. Inclui o autor, o número da versão e a data de submissão. A metadata abrangente facilita a gestão de documentos e permite que as Agências Regulamentares rastreiem as alterações e garantam a integridade dos dados.
Garantir a Consistência
A consistência é essencial para uma submissão eCTD bem-sucedida. Todos os documentos devem ser consistentes em termos de conteúdo, formatação e metadata. A consistência garante que a submissão é fácil de navegar e minimiza a possibilidade de erros durante a revisão regulamentar.
Rever e Validar
Antes de submeter o pacote eCTD, é essencial rever e validar a submissão quanto à sua completude e exatidão. Uma revisão minuciosa garante que todos os documentos necessários estão incluídos e que não existem erros ou discrepâncias. A validação garante que a submissão está em conformidade com as especificações e os requisitos regulamentares do eCTD.
Comunicar com a Agência Reguladora
As agências regulamentares fornecem diretrizes e feedback sobre as submissões eCTD. É importante esclarecer dúvidas ou preocupações levantadas pelas Autoridades de Saúde antes de submeter o pacote. É também essencial responder prontamente às questões que a Agência Regulamentar levanta durante o processo de revisão.
Em conclusão, seguir as melhores práticas é crucial para as submissões eCTD. Ao fazê-lo, pode garantir um processo de submissão suave, simplificado e bem-sucedido que cumpre todos os requisitos Regulamentares e acelera o processo de revisão.
Integre Freyr SUBMIT PRO e cumpra todos os seus requisitos de submissão eCTD. A ferramenta eCTD está totalmente equipada com funcionalidades personalizadas e únicas que tornam o processo mais fluido e eficiente.
Diga adeus às submissões stressantes e olá às submissões regulamentares sem stress com Freyr SUBMIT PRO!









