Os custos de conformidade para as empresas farmacêuticas podem representar até 25% das suas despesas operacionais totais. As empresas farmacêuticas com múltiplos portefólios de produtos enfrentam desafios únicos na gestão da conformidade global, no acompanhamento das submissões de dossiês e na supervisão das variações de rotulagem. A complexidade dos requisitos regulamentares em diferentes regiões, juntamente com o manuseamento manual de grandes volumes de dados, pode levar à não conformidade, atrasos nas aprovações de mercado e ineficiências operacionais.
Este blog explora os principais desafios que as empresas farmacêuticas encontram ao gerir múltiplos portefólios de produtos e demonstra como o software regulamentar, apoiado por estudos de caso reais, oferece uma solução estratégica para estes problemas.
Principais Desafios na Gestão de Múltiplos Portefólios de Produtos
- Requisitos Complexos de Conformidade Global: Cada país tem o seu próprio organismo regulador, e os seus requisitos podem variar drasticamente. Por exemplo, a US FDA, a EMA e a PMDA do Japão têm diferentes formatos de submissão, prazos e padrões de conformidade. As empresas farmacêuticas devem gerir diversos dossiês em várias regiões, garantindo que não há desvios das regulamentações locais.
- Acompanhamento das Variações de Rótulos entre Regiões: Gerir as variações de rótulos para diferentes regiões e garantir atualizações atempadas é um dos aspetos mais desafiadores da gestão de portefólio. Uma má gestão das alterações de rótulos pode levar à não conformidade, recolhas de produtos e grandes reveses financeiros.
- Sobrecarga na Submissão de Dossiês: A submissão e gestão de dossiês para várias linhas de produtos, cada uma em fases de desenvolvimento distintas, pode sobrecarregar rapidamente as equipas internas. Gerir manualmente as atualizações do ciclo de vida dos produtos resulta frequentemente em erros e atrasos nas aprovações.
- Má Gestão de Recursos: As equipas muitas vezes têm dificuldade em alocar os recursos certos de forma eficiente. Sem um sistema de gestão robusto, as empresas podem sobrecarregar o pessoal com tarefas administrativas, limitando a sua capacidade de se concentrarem em atividades estratégicas essenciais.
- Silos de Dados: A falta de centralização significa que os dados relacionados com submissões, aprovações e atualizações de produtos são armazenados em sistemas díspares, o que leva a ineficiências, falhas de comunicação e dificuldade em manter uma visão holística do ciclo de vida do produto.
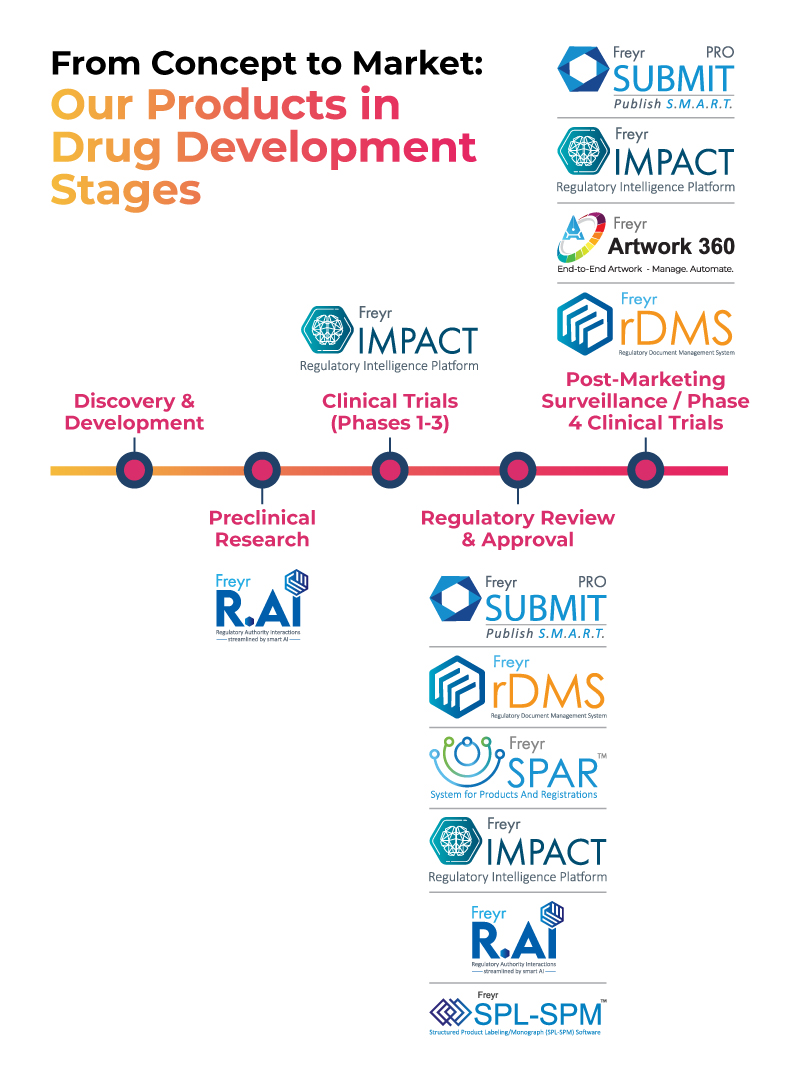
O conjunto de produtos tecnológicos da Freyr Digital apoia as empresas farmacêuticas desde o conceito até ao mercado, conforme ilustrado na imagem abaixo.
Estudos de Caso: Como o Software de Regulamentação Oferece Vantagem Estratégica
Ao adotar software regulamentar, as empresas farmacêuticas podem automatizar processos, garantir a conformidade e, em última análise, obter uma vantagem estratégica sobre os concorrentes. Os seguintes estudos de caso destacam exemplos reais de como as nossas soluções de software regulamentar ajudaram as empresas farmacêuticas a superar estes desafios.
Caso Comprovado
Desafio do Cliente
Uma empresa farmacêutica de genéricos com sede nos US estava com dificuldades em gerir eficientemente as suas submissões regulamentares End-to-End e a gestão de documentos. Enfrentaram desafios com repositórios de documentos dispersos, dificultando o acesso contínuo a documentos regulamentares para partes interessadas internas e externas. Além disso, o processo de criação e gestão de Structured Product Labeling (SPL) era complexo, levando a atrasos nos prazos de submissão e ao aumento dos ciclos de revisão.
A Solução da Freyr Digital
A Freyr Digital interveio como fornecedor de soluções virtuais de Assuntos Regulamentares, implementando estes três produtos chave como soluções para responder aos desafios do cliente:
- Freyr rDMS: Um sistema centralizado de gestão de documentos para atuar como a única fonte de verdade para todas as submissões e documentos regulamentares, garantindo acesso em tempo real e controlo de versões para equipas internas e parceiros externos.
- Freyr SUBMIT PRO: Uma ferramenta poderosa para publicação e submissão eCTD, otimizando o processo de submissão, reduzindo o tempo de preparação e garantindo a conformidade com os padrões regulamentares em evolução.
- Freyr SPL-SPM: Uma solução eficiente para gerir todas as atividades relacionadas com SPL, melhorando significativamente os processos de criação, gestão e submissão de documentos.
Resultados
Ao implementar estas soluções, a Freyr Digital ajudou o cliente a alcançar:
- Uma redução de 30% no tempo de preparação da submissão
- 100% de conformidade com todos os requisitos regulamentares
- Uma melhoria de 40% na eficiência do processamento de documentos
- Uma redução de 25% nos ciclos de revisão
Conclusão: Adotar a Transformação Digital para o Sucesso Estratégico
Gerir múltiplos portefólios de produtos em mercados globais não é uma tarefa fácil. No entanto, com o software de regulamentação adequado, as empresas farmacêuticas podem otimizar os processos, garantir a conformidade e obter uma vantagem estratégica na indústria.
O conjunto de ferramentas regulamentares da Freyr Digital – incluindo Freyr SUBMIT PRO, Freyr rDMS e Freyr SPL-SPM – tem ajudado consistentemente as empresas farmacêuticas a reduzir os tempos de submissão, a melhorar a conformidade e a otimizar os recursos. Ao automatizar processos manuais, fornecer gestão de dados centralizada e oferecer informações em tempo real, as nossas soluções capacitam as empresas farmacêuticas a manterem-se à frente num mercado competitivo. Fale connosco.









