Ninsho (certificação de dispositivos médicos) é um sistema de certificação por terceiros no Japão, no qual um Organismo de Certificação Registado (RCB), acreditado pelo Ministro da Saúde, Trabalho e Bem-Estar (MHLW), certifica dispositivos médicos designados de alto controlo. É aplicável a dispositivos de Classe II e a um número limitado de dispositivos de Classe III que possuem uma Norma Industrial Japonesa (JIS) associada. Alguns dispositivos médicos de Classe II sem critérios de certificação estabelecidos requerem aprovação ao abrigo do programa Shonin.
Quais são as outras Vias de Registo de Dispositivos no Japão?
No Japão, as vias Todokede e Shonin também são utilizadas para aprovações de dispositivos médicos, além do Ninsho. Dependendo da categoria de risco do dispositivo e da disponibilidade de precedentes no Japão, o fabricante deve planear cuidadosamente a sua submissão do dispositivo.
Quais são os Pré-requisitos para a Certificação Ninsho?
Os fabricantes que registam os seus dispositivos através da via Ninsho devem planear meticulosamente as submissões em termos do seguinte:
- Seleção de um RCB
- Submissão de dados gerais do dispositivo, tais como categoria do dispositivo médico, utilização prevista, dados de análise de risco de eficácia, dados clínicos, etc.
- Fornecimento do Resumo da Documentação Técnica (STED)
- O fornecimento de documentos deve ser apenas em japonês.
- Os fabricantes estrangeiros devem nomear obrigatoriamente um Titular da Autorização de Introdução no Mercado (MAH) ou um Titular da Autorização de Introdução no Mercado Designado (DMAH)
- Os fabricantes estrangeiros devem registar-se junto do MHLW e obter um certificado de Registo de Fabricante Estrangeiro (FMR) para os seus estabelecimentos de fabrico
O que são os RCBs?
Os Organismos de Certificação Registados (RCB) são organismos de certificação por terceiros acreditados pelo MHLW. Os RCB são responsáveis por rever e certificar dispositivos médicos elegíveis e aplicados ao abrigo da via Ninsho. Os RCB são também responsáveis pela realização da auditoria ao Sistema de Gestão da Qualidade (QMS) da instalação do fabricante.
Quais são os Requisitos de SGC para o Registo de Dispositivos ao abrigo da Via Ninsho?
Os fabricantes devem cumprir todos os requisitos do SGQ definidos na Portaria 169. O MAH ou o DMAH devem submeter a submissão aos RCBs. Os RCBs realizarão uma inspeção detalhada do SGQ nas instalações do fabricante e, após a implementação satisfatória do SGQ, emitirão o certificado.
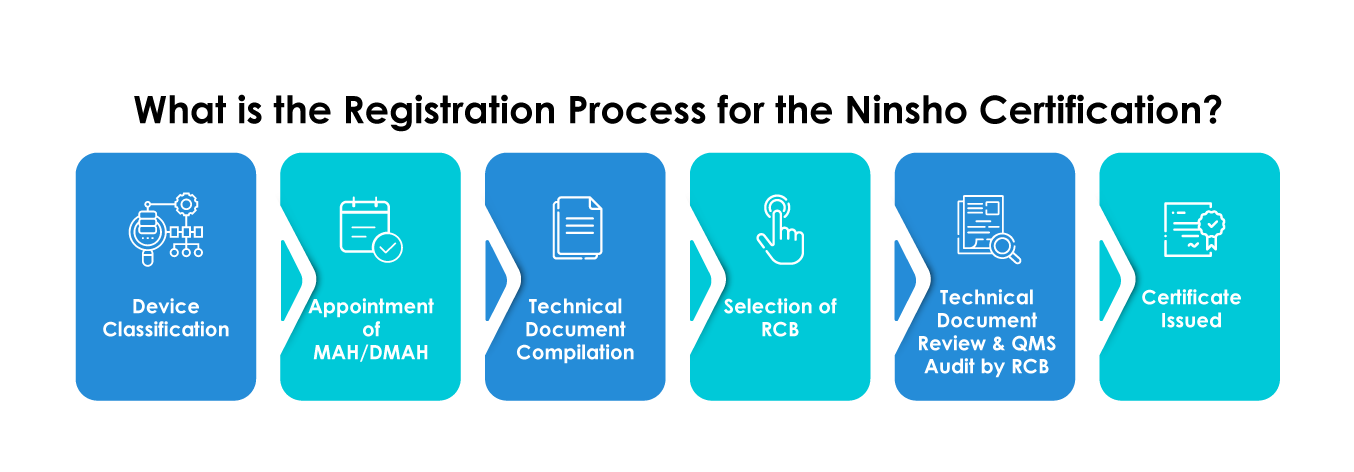
Qual é o Prazo Médio Necessário para a Certificação Ninsho?
O RCB normalmente necessita de três (03) a cinco (05) meses para concluir a avaliação técnica, executar a auditoria de QMS e emitir o certificado Ninsho.
Existe algum Prazo de Validade para a Certificação Ninsho?
O registo de dispositivos médicos não expira, mas o promotor deve renovar os certificados QMS a cada cinco (05) anos.
O Japão, sendo o terceiro maior mercado de dispositivos médicos depois dos EUA e da China, oferece grandes oportunidades para fabricantes de dispositivos médicos em todo o mundo. Os fabricantes que desejam comercializar os seus dispositivos no Japão devem planear cuidadosamente a certificação e aprovação de dispositivos médicos, uma vez que a PMDA tem requisitos regulamentares específicos. Os fabricantes podem optar por um parceiro regulamentar fiável para um acesso sem complicações ao mercado japonês.
Para saber mais sobre a certificação de dispositivos médicos no Japão ou quaisquer outros regulamentos da PMDA Japão, Contacte a Freyr Hoje!
