
O software de dispositivos médicos na Coreia do Sul é utilizado para diagnosticar, tratar e monitorizar pacientes no sistema de saúde moderno. Inclui tanto software incorporado, que é integrado em dispositivos médicos, como software autónomo, que pode ser utilizado em PCs, dispositivos móveis e serviços baseados na web. O Ministério da Segurança Alimentar e Medicamentosa (MFDS) da Coreia do Sul é responsável por regulamentar o software de dispositivos médicos e garantir a sua segurança e eficácia. A 5 de julho de 2023, o MFDS estabeleceu critérios para a aprovação e inspeção de software de dispositivos médicos; estas regulamentações fornecem uma estrutura que os requerentes podem seguir ao submeter software para aprovação ou revisão.
Os regulamentos abordam uma variedade de assuntos, incluindo o âmbito da submissão, os requisitos de documentação técnica e os relatórios de verificação de conformidade. Existem normas e diretrizes internacionais que se aplicam ao software de dispositivos médicos, além das diretrizes da MFDS, como a norma IEC (International Electrotechnical Commission) 62304 para processos de ciclo de vida de software e a orientação da United States Food and Drug Administration (US FDA) sobre submissões médicas móveis.
Plano de Desenvolvimento de Software e Análise de Requisitos
- O Plano de Desenvolvimento de Software delineia a abordagem geral ao desenvolvimento de software, incluindo especificações, métodos e ferramentas de desenvolvimento. Abrange também a verificação, a gestão de riscos de dispositivos médicos, a gestão de configuração e a documentação.
- A Análise de Requisitos estabelece os requisitos do software de dispositivos médicos, incluindo medidas de controlo de risco e métodos de verificação. Ao planear e analisar cuidadosamente o processo de desenvolvimento de software, os programadores podem garantir que o software resultante cumpre os padrões necessários de segurança e eficácia.
- O Relatório de Verificação de Conformidade do Software inclui um resumo do plano de desenvolvimento de software, o número de controlo de documentos do fabricante e uma visão geral da análise de requisitos. Ao aderir a estas diretrizes, o software de dispositivos médicos pode ser desenvolvido com confiança, sabendo que foi submetido a testes rigorosos e que cumpre os padrões necessários de segurança e eficácia.
Verificação e Validação de Software de Dispositivos Médicos
- A Verificação de Software de Dispositivos Médicos garante que o software cumpre os requisitos especificados.
- A Validação de Software de Dispositivos Médicos garante que o software satisfaz as necessidades do utilizador e as utilizações pretendidas.
- O Relatório de Verificação e Validação de Software de Dispositivos Médicos descreve o processo de verificação e validação, incluindo o nome do produto, a revisão e os nomes dos indivíduos que examinaram e aprovaram o relatório. O relatório pode variar, dependendo das características do software, mas deve incluir uma descrição do software, os métodos de verificação e validação utilizados e os resultados dos testes.
Ambiente Operacional e Software de Origem Desconhecida (SOUP)
- Se o software depender de hardware específico, como software incorporado, o documento técnico deve descrever as especificações do hardware.
- No entanto, se o software for autónomo e desenvolvido para funcionar em hardware de uso geral, o ambiente operacional deve ser descrito na documentação. Isto inclui as especificações mínimas recomendadas, como Microsoft Windows 10 ou superior.
- Além disso, se o software do dispositivo médico incluir Software de Origem Desconhecida (SOUP) comercial, deve ser criado um ambiente operacional para garantir o seu bom funcionamento. Ao descrever cuidadosamente o ambiente operacional e abordar qualquer SOUP, os programadores podem garantir que o software dos seus dispositivos médicos é seguro e eficaz para a sua utilização pretendida.
Gestão de Riscos de Dispositivos Médicos e Requisitos de Documentação
- O processo de gestão de risco de software como dispositivo médico inclui a identificação de situações perigosas, o estabelecimento de medidas de controlo de risco, a verificação dessas medidas e a gestão de alterações de software.
- O documento de gestão de riscos de software MFDS-RM fornece informações sobre a gestão de riscos de software.
- Além disso, os requisitos de documentação são essenciais para garantir que o software cumpre os padrões necessários de segurança e eficácia.
- O plano de desenvolvimento de software, a análise de requisitos de software de dispositivos médicos e os relatórios de verificação e validação de software devem ser incluídos na documentação.
- O Relatório de Verificação de Conformidade do Software delineia os requisitos de documentação; inclui também um resumo dos documentos aplicáveis e o número de controlo de documentos do fabricante.
Figura 1: Processo de Gestão de Riscos de Dispositivos Médicos
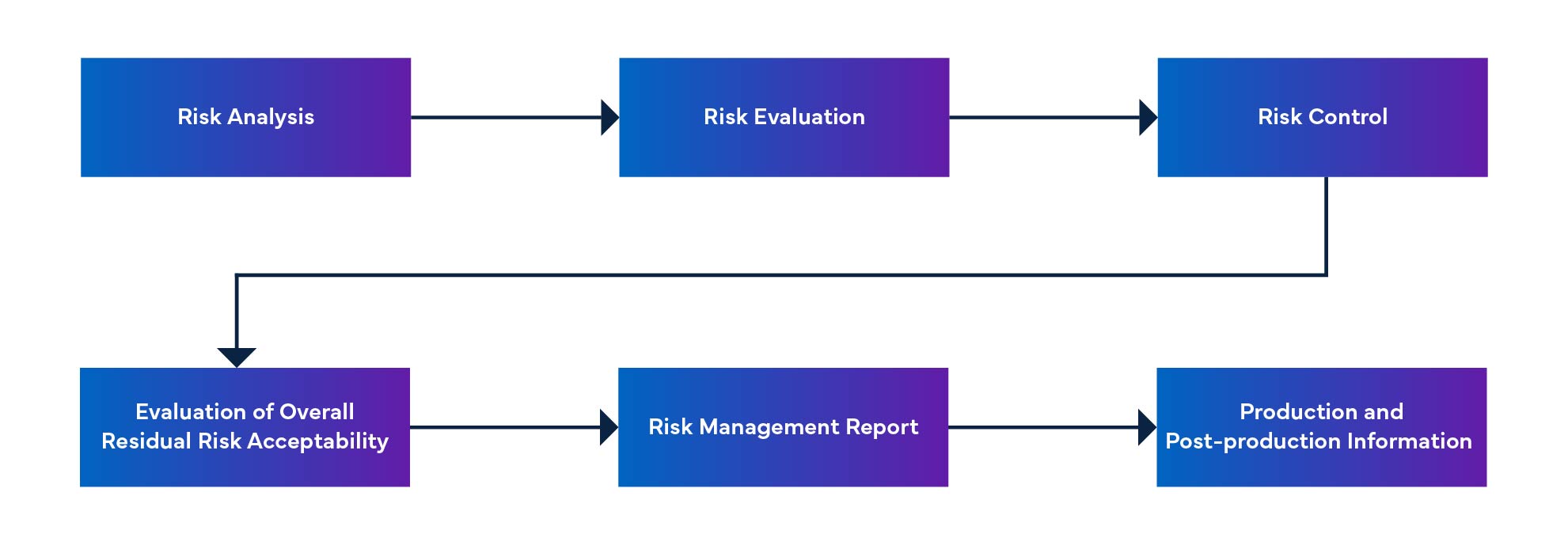
Anomalias Não Resolvidas e Ações Corretivas para Software SaMD
- O documento MFDS-PR (Resolução de Problemas de Software) delineia o processo de resolução de problemas de software, que inclui a comunicação de problemas, análise, implementação e verificação.
- O documento inclui também uma lista de problemas não resolvidos, bugs, defeitos e anomalias, bem como uma avaliação de risco residual para o sistema de software.
- As ações corretivas tomadas para resolver estas questões devem ser documentadas no plano de manutenção de software, que é estabelecido de acordo com o processo de manutenção de software.
- O documento de manutenção da MFDS fornece informações sobre a manutenção e resolução de problemas de software SaMD.
Revisão de Documentos Técnicos e Requisitos de Submissão para Software SaMD
Os principais documentos de revisão durante o processo de revisão são dados de desempenho, relatório de confirmação de conformidade e dados de verificação e validação de software de dispositivos médicos, a Especificação de Design de Software (SDS), a Declaração de Requisitos de Software de dispositivos médicos (SRS), e os relatórios de verificação e validação. O Relatório de Confirmação de Conformidade e o Relatório de Verificação e Validação de Software de Dispositivos Médicos devem ser submetidos.
Gestão de Risco de Software para Dispositivos Médicos
- Identificar perigos potenciais associados ao software e à sua utilização.
- Avaliação da gravidade dos riscos associados a estes perigos.
- Implementar medidas de controlo de risco para minimizar a probabilidade de dano.
- Monitorizar e rever a eficácia destas medidas de controlo de risco.
- Documentar todas as atividades e decisões de gestão de risco de dispositivos médicos.
Num sistema de software, os itens de software são divididos em partes mais pequenas, incluindo itens de software detalhados. Quando um item não pode ser mais dividido, é chamado de unidade. O sistema permite a divisão até ao nível da unidade, ajudando a determinar o nível de segurança para cada item de software. Ao juntar estes itens de software, conseguimos determinar o nível de segurança para todo o sistema de software.
Figura 2: Desagregação e Integração de Software de Dispositivos Médicos
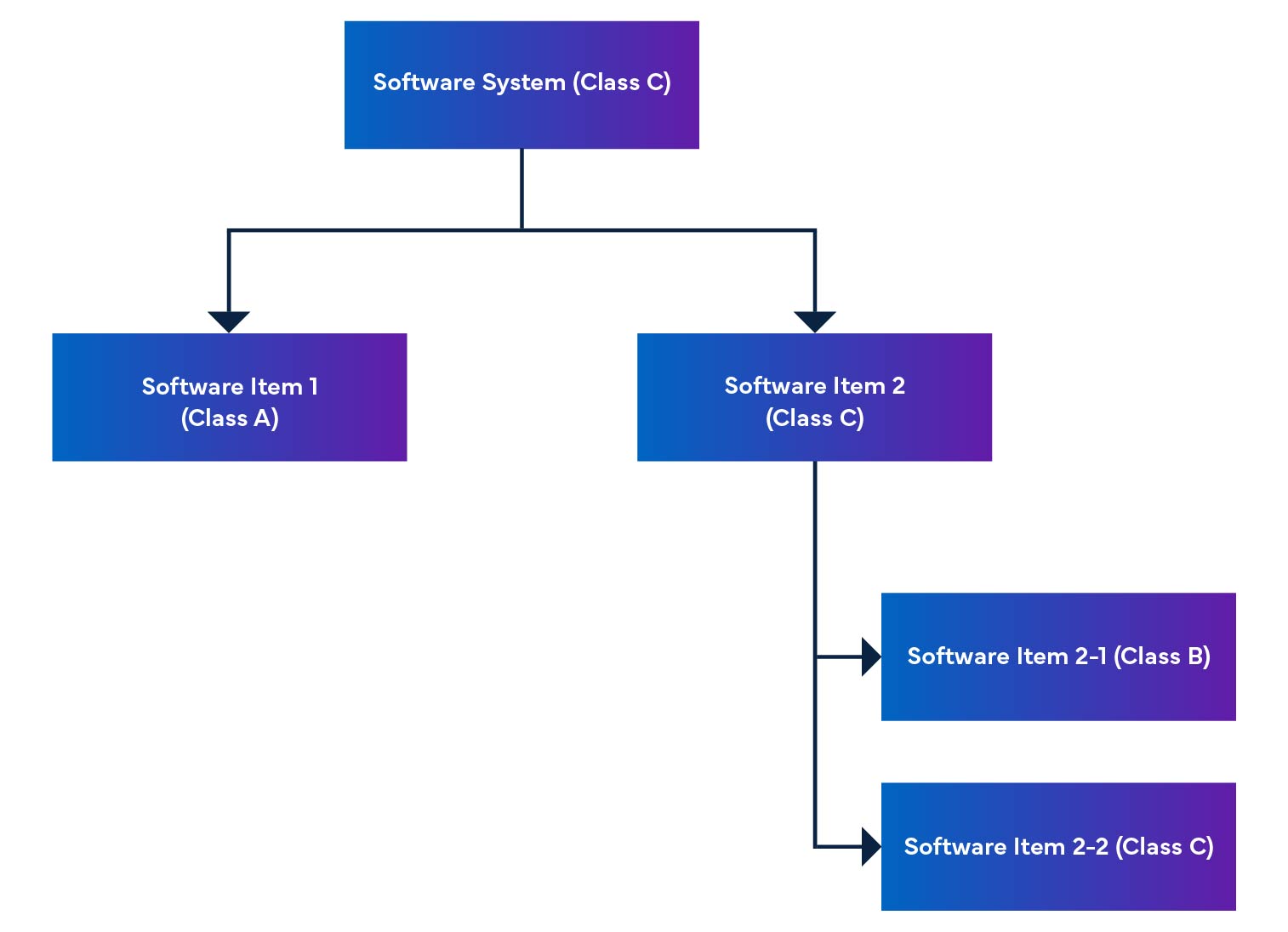
O regulamento também menciona a classificação de segurança do software, que é uma classificação para identificar os riscos do software SaMD (ver Tabela 1).
Tabela 1: Definição de Classificação de Segurança
| Classificação | Definição de Classe de Segurança de Software para Dispositivos Médicos |
| Classe A | Sem possibilidade de lesão ou dano corporal. |
| Classe B | Lesões menos graves (lesões menores) são prováveis. |
| Classe C | Possibilidade de lesão grave ou morte. |
Gestão da Configuração de Software
- Manter documentação precisa e atualizada para todas as versões, alterações e atualizações de software.
- Garantir que toda a documentação seja devidamente revista e aprovada.
- Implementar procedimentos para gerir alterações na configuração do software.
- Documentar todas as atividades e decisões de gestão da configuração de software.
Manutenção de Software
- Testar e monitorizar regularmente o software para garantir que permanece seguro e eficaz para o seu uso pretendido.
- Implementar procedimentos para resolver quaisquer problemas que possam surgir, incluindo correções de erros e atualizações de software.
- Documentar todas as atividades e decisões de manutenção de software.
Resolução de Problemas
- Identificar a causa raiz do problema.
- Implementar ações corretivas para resolver o problema.
- Documentação de todo o processo de resolução de problemas para consulta futura.
Ao seguir as diretrizes acima, os programadores podem garantir que quaisquer problemas com o software dos seus dispositivos médicos são devidamente abordados e documentados, e que o software cumpre os requisitos necessários para aprovação ou exame.
Se é um fabricante de dispositivos médicos que procura a conformidade com os padrões de software de dispositivos médicos da Coreia do Sul, os especialistas regulamentares da Freyr podem guiá-lo através do complexo panorama regulamentar do país. Garantiremos que os seus dispositivos estejam alinhados com os mais recentes regulamentos de dispositivos médicos da Coreia do Sul para uma conformidade sem problemas. Fale connosco para saber mais!










