24 de setembro de 2016; com o prazo, a apenas um mês, para a conformidade com o Identificador Único de Dispositivo (UDI) para dispositivos de Classe II, é nossa suposição, se não certeza, que todos os fabricantes de dispositivos médicos estão bem equipados com um roteiro regulamentar abrangente. Além de terem um controlo firme sobre os pré-requisitos de governação, espera-se que os fabricantes estejam preparados para auditorias de conformidade. Desde a validação dos registos do Identificador de Dispositivo (DI) e do Identificador de Produto (PI) até às submissões bem-sucedidas no GUDID, eles devem ter conhecimento sobre os dados a submeter e os procedimentos a seguir. Quer seja antes ou depois da submissão, estar equipado com um melhor conhecimento do saber-fazer processual pode proteger os fabricantes dos desafios correspondentes relacionados com a agregação de dados, a submissão de registos DI e a gestão de relatórios de dispositivos, o acompanhamento de reconhecimentos da HA, etc.
Para equipar os fabricantes com uma melhor posição em tais cenários, aqui fornecemos um infográfico de fácil compreensão sobre os desafios e soluções da conformidade UDI, que poderá poupar o seu tempo a decifrar as complexidades da conformidade e a planear e estruturar melhor o roteiro.
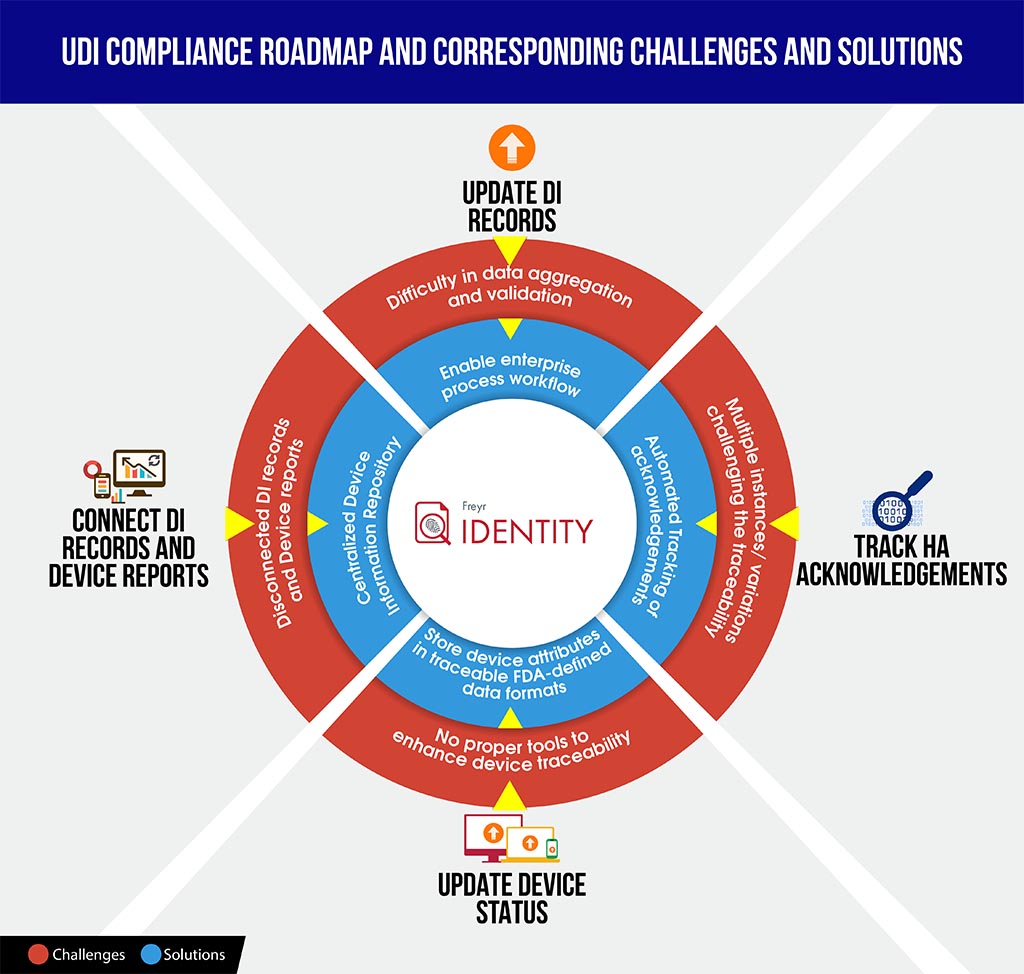
Para guiar a sua organização de forma eficiente através deste complexo processo de conformidade, a Freyr oferece o melhor de dois mundos – uma solução de software UDI sob demanda, totalmente configurável, Freyr IDENTITY, bem como um Centro de Excelência (CoE) em UDI que oferece serviços UDI de excelência, económicos e personalizáveis, concebidos para as suas necessidades únicas e exigentes.









