As autoridades sanitárias de todos os países, com exceção do Canadá, exigem que todos os fabricantes estrangeiros de dispositivos médicos nomeiem um representante local, no próprio país ou um representante autorizado. A função de um representante legal é representar o fabricante e o dispositivo no país de destino e servir de elo de ligação entre as autoridades sanitárias e os fabricantes estrangeiros. Existe terminologia específica para cada país para designar o representante local. Nos EUA, o representante local é designado por US , enquanto no Reino Unido é referido como UKRP Pessoa Responsável no Reino Unido). No Sri Lanka, o representante local é designado por «Agente Local do Sri Lanka» ou «Representante Autorizado do Sri Lanka», sendo também Autorização de Introdução no Mercado (MAH) do dispositivo.
Os fabricantes estrangeiros de dispositivos médicos podem optar por nomear o seu distribuidor como agente local, o qual, por defeito, seria também o Titular da Autorização de Introdução no Mercado (MAH). No entanto, recomenda-se nomear um prestador de serviços independente, sem conflitos de interesses, como seu MAH. As vantagens de nomear um prestador de serviços independente como seu MAH mencionadas abaixo. Um MAH :
- Ser competente nos Assuntos Regulamentares do país e nos requisitos de PMS
- Alcançar os objetivos de negócio nomeando vários distribuidores para a penetração no mercado.
- Capacidade de focar-se na conformidade regulamentar
- Tecnicamente competente para responder às questões levantadas pela Agência
- Rótulos comuns para um único MAH o país
- Evitar as complicações decorrentes da necessidade de atualizar os rótulos em caso de mudança de distribuidor, que também atuaria como titular da autorização de introdução no mercado (MAH) ou agente MAH
Em alguns países, por exemplo, na Índia, não existe qualquer disposição que permita a transferência da autorização de introdução no mercado, sendo necessária submissão um novo submissão . Em contrapartida, no Sri Lanka, a Autoridade Nacional de Regulamentação de Medicamentos (NMRA) permitea transferência do titular da MAH . O principal desafio que os fabricantes estrangeiros de dispositivos enfrentam ao alterar o MAH a exigência de apresentar um Certificado/Carta de Não Objeção (NoC/NoL) do atual MAH ativo. A NMRA também facilita a MAH MAH , mesmo quando MAH relutante em emitir um NoC.
A alteração do nome e/ou endereço do titular MAH Sri Lanka não MAH considerada uma transferência da autorização de introdução no mercado se o titular for a mesma pessoa/entidade, devendo essa alteração ser notificada através de submissão de alteração pós-aprovação. O fabricante deverá contactar diretamente a NMRA caso pretenda alterar os dados do MAH no submissão, que ainda se encontre em fase de análise pela NMRA.
A necessidade de transferir uma Autorização de Introdução no Mercado MAH Autorização de Introdução no Mercado MAH em situações em que o fabricante decide alienar a atual Autorização de Introdução no Mercado quando a atual AIM é adquirida por outra entidade jurídica. O MAH ser transferida é designado por «cedente» e a empresa, sociedade, pessoa ou entidade jurídica a quem a transferência é concedida é designada por «cessionária».
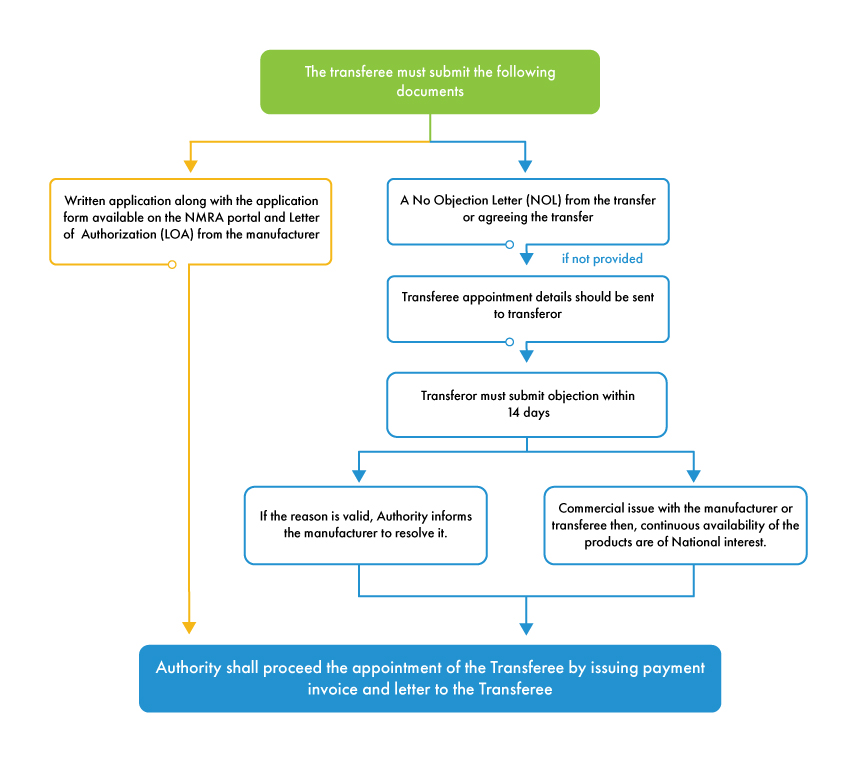
Para que o processo MAH tenha início, o cedente deve emitir uma Carta de Não Objeção (NOL) concordando com a transferência. Se o cedente se recusar a emitir a NOL, a autoridade concede um prazo de 14 dias para a apresentação de objeções contra a nomeação do cessionário (novo MAH). Se o motivo da objeção for válido e disser respeito ao fabricante, a autoridade notifica o fabricante para que resolva a objeção e dá continuidade ao processo de transferência. Se o cedente tiver algum conflito comercial com o cessionário ou com o fabricante, a NMRA dará continuidade ao processo de transferência, uma vez que a autoridade está mais preocupada com a disponibilidade do dispositivo no mercado do Sri Lanka do que com quaisquer obrigações comerciais entre as várias partes interessadas.
Ao contrário do que acontece noutros países, a regulamentação da NMRA é favorável aos fabricantes estrangeiros no que diz respeito MAH . A NMRA permite MAH mediante a apresentação de toda a documentação necessária, a menos que a objeção levantada pelo cedente seja substancial e genuína. É vantajoso para todos os fabricantes estrangeiros nomear um MAH independente, MAH evitar quaisquer complicações no Autorização de Introdução no Mercado dos seus produtos no Sri Lanka. O apoio de um agente local para dispositivos médicos no Sri Lanka serve de plataforma para que todos os fabricantes estrangeiros nomeiem e alterem o MAH , com a documentação adequada.
ParaMAH de agente local/titular da autorização de introdução no mercado (MAH ) ou para serviços MAH no Sri Lanka, reach um especialista regional em regulamentação. Mantenha-se informado. Mantenha-se em conformidade.









