
No atual panorama farmacêutico altamente regulamentado, manter a conformidade com as Boas Práticas (GxP) não é apenas uma necessidade legal, mas sim um compromisso com a segurança dos doentes e a qualidade dos produtos. À medida que as autoridades reguladoras em todo o mundo, incluindo a FDA EMA, intensificam a sua atenção aos controlos de fabrico e à consistência dos produtos, a Verificação Contínua do Processo (CPV) surgiu como uma metodologia transformadora para garantir GxP contínua GxP ao longo de todo o ciclo de vida do produto.
Compreender a verificação contínua de processos
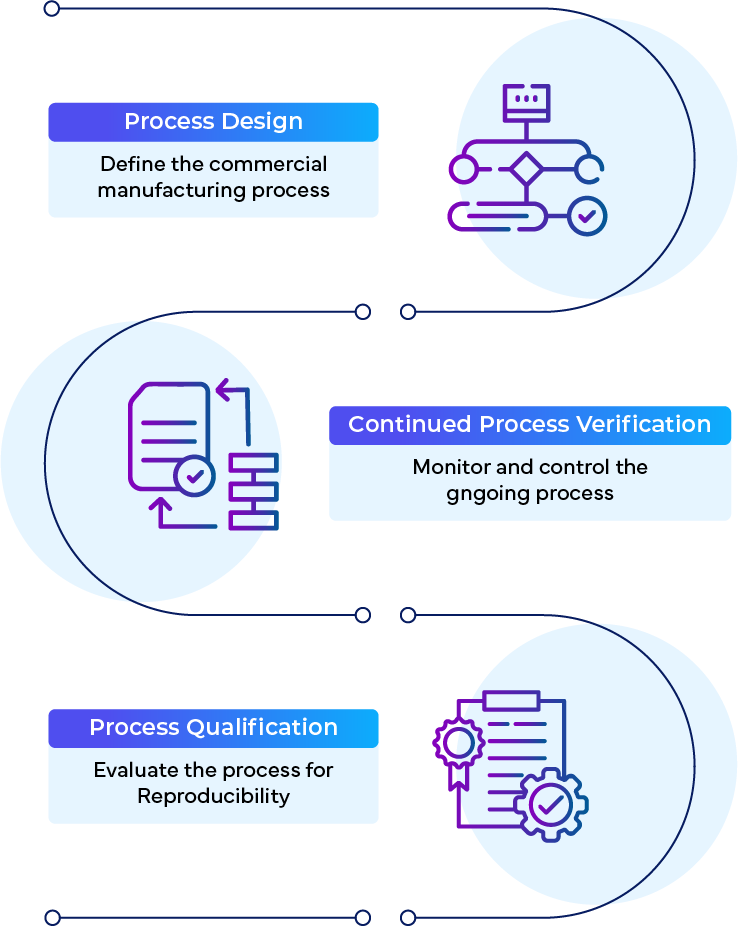
A CPV é uma (1) das três (3) fases da diretriz de validação de processos FDA:
- Concepção de Processos
- Qualificação do processo
- Verificação contínua do processo
Ao contrário das abordagens tradicionais de validação, que muitas vezes dependem fortemente de dados limitados provenientes de lotes pré-comercialização, a CPV privilegia a recolha de dados em tempo real e a análise de tendências durante a produção de rotina. Esta transição de uma gestão da qualidade reativa para uma proativa permite aos fabricantes detetar desvios no processo, mitigar riscos numa fase precoce e manter um estado validado ao longo de toda a vida útil do produto.
Por que o CPV é uma revolução
- Garantia de qualidade em tempo real
Ao recolher e analisar dados durante cada ciclo de produção, o CPV facilita a deteção imediata de anomalias. Esta informação em tempo real permite tomar decisões mais rápidas, reduzindo o risco de lançar produtos abaixo dos padrões de qualidade e evitando recalls dispendiosos. - Reforçado Conformidade regulamentar
As autoridades reguladoras esperam cada vez mais que as empresas farmacêuticas implementem abordagens de ciclo de vida para a validação. O CPV apoia esta expectativa, demonstrando um estado contínuo de controlo, alinhando-se com as diretrizes ICH , Q9 e Q10 e garantindo a conformidade com os requisitos globais de conformidade. - Otimização de custos
Embora a implementação do CPV exija um investimento inicial em tecnologias analíticas e formação, acaba por reduzir os custos a longo prazo. Minimiza a necessidade de revalidações frequentes, diminui as rejeições de lotes e melhora a eficiência da produção. - Tomada de decisões baseada em dados
A CPV recorre a ferramentas estatísticas avançadas e à automatização para processar grandes volumes de dados. Esta abordagem estruturada à gestão de dados contribui para o planeamento estratégico, a melhoria contínua e a gestão informada dos riscos — pilares dos sistemas de qualidade modernos.
Melhores práticas de implementação
1. Definir Parâmetros Críticos do Processo (CPPs)
Comece por identificar e estabelecer os CPPs e os Atributos Críticos de Qualidade (CQAs) com base em dados históricos e experimentais. Estas métricas servem de base para a monitorização em tempo real.
2. Aproveite as ferramentas digitais e a automatização
Integre o software CPV com os seus Sistemas de Execução da Produção (MES) e Sistemas de Gestão de Informação Laboratorial (LIMS). A automatização melhora a precisão dos dados, a frequência e a visualização de tendências.
3. Colaboração interfuncional
A implementação bem-sucedida do CPV requer coordenação entre as equipas de Garantia da Qualidade, Produção e TI. O estabelecimento de uma estratégia unificada de CPV garante a consistência e a responsabilidade partilhada.
4. Desenvolver modelos robustos de análise de dados
Utilizar o controlo estatístico de processos (SPC), a análise multivariável e algoritmos de aprendizagem automática para analisar tendências, prever desvios e apoiar a melhoria contínua.
5. Alinhamento regulamentar
Documente todos os aspetos do seu processo de CPV e certifique-se de que o seu sistema está preparado para uma auditoria. Alinhe a sua documentação e práticas com as expectativas regulamentares globais.
O CPV em ação: um exemplo prático
Considere uma empresa farmacêutica que fabrica injetáveis estéreis. Antes da implementação do CPV, os seus esforços de validação centravam-se principalmente em três (3) lotes pré-comercialização. As variações pós-comercialização passavam frequentemente despercebidas até surgirem reclamações sobre o produto.
Ao adotar o CPV, a empresa instalou sensores de temperatura e pressão em tempo real ao longo de toda a sua linha de produção. Os dados foram analisados continuamente através de gráficos de SPC. Como resultado, identificaram um desvio menor, mas recorrente, no volume de enchimento, com antecedência suficiente para tomar medidas corretivas antes que o desvio afetasse a qualidade do produto. Esta mudança não só garantiu GxP , como também reduziu significativamente o tempo de inatividade e a necessidade de retrabalho do produto.
Conclusão
A verificação contínua dos processos é mais do que um mero requisito regulamentar. Trata-se de uma abordagem estratégica para garantir a qualidade consistente dos produtos, a eficiência operacional e a conformidade com GxP em constante evolução. Com as ferramentas certas, a mentalidade adequada e a orientação de especialistas, as empresas farmacêuticas podem transformar os seus programas de validação e promover uma conformidade sustentada.
Deixe que a Freyr o guie na sua jornada com o CPV
Na Freyr, somos especializados em serviços end-to-end e conformidade para a indústria farmacêutica. Quer esteja apenas a dar os primeiros passos na implementação do CPV ou pretenda melhorar o seu sistema atual, os nossos especialistas podem ajudá-lo a conceber, implementar e validar estruturas de CPV robustas e adaptadas às suas necessidades.
Pronto para melhorar GxP sua GxP ? Contacte a Freyr hoje mesmo para saber como podemos ajudar a preparar as suas operações farmacêuticas para o futuro.










