Ao longo dos anos, com os avanços do software e da digitalização, tem havido uma mudança sísmica na forma como os dispositivos médicos são administrados e entregues. A integração de software com dispositivos médicos aumentou rapidamente e está a impulsionar avanços incríveis no fornecimento de soluções de saúde em vários domínios, como o diagnóstico, a prevenção de doenças e o tratamento de lesões ou doenças.
No entanto, o efeito do software na segurança e desempenho de dispositivos médicos tem sido duvidoso, particularmente, quando o próprio dispositivo é um produto apenas de software. Assim, os regulamentos de software de dispositivos médicos são constantemente revistos para determinar a consideração de software como dispositivo médico (SaMD). Recentemente, o conselho consultivo da Comissão Europeia - Medical Device Coordination Group (MDCG) - focou-se em melhorar os regulamentos de software de dispositivos médicos e publicou uma orientação que descreve a abordagem a ser aplicada, ao determinar se um software é um dispositivo médico ou não. O que delineia a orientação? Vejamos.
O Âmbito da Orientação
A orientação MDCG abrange tanto o software de dispositivos médicos como o software de dispositivos médicos para diagnóstico in vitro (IVD). De acordo com o documento, um Software de Dispositivos Médicos (MDSW) é definido como um software destinado a ser utilizado isoladamente ou em combinação, para um fim especificado na definição de “dispositivo médico” no Regulamento dos Dispositivos Médicos 2017/745 (MDR) ou no Regulamento dos Dispositivos Médicos para Diagnóstico In Vitro 2017/746 (IVDR). Descreve os critérios a aplicar para determinar se um software sujeito a revisão é ou não um dispositivo médico e pretende fornecer esclarecimentos e recomendações adicionais sobre o MDSW para fabricantes de dispositivos médicos e outras partes interessadas.
Em primeiro lugar, a orientação estabelece os termos mais importantes utilizados no contexto do MDSW, que incluem:
Finalidade prevista: A utilização a que se destina um dispositivo de acordo com os dados fornecidos pelo fabricante no rótulo, nas instruções de utilização, ou em materiais ou declarações promocionais ou de vendas e conforme especificado pelo fabricante na avaliação clínica.
Acessório: Um artigo que, embora não sendo ele próprio um dispositivo médico, é destinado pelo seu fabricante a ser utilizado em conjunto com um ou vários dispositivos médicos para permitir especificamente que o(s) dispositivo(s) médico(s) seja(m) utilizado(s) de acordo com a(s) sua(s) finalidade(s) prevista(s) ou para auxiliar a funcionalidade do(s) dispositivo(s) médico(s) especificamente e diretamente em termos da(s) sua(s) finalidade(s) prevista(s). Além disso, o MDCG menciona que o acessório de software pode estar a impulsionar ou a influenciar a utilização de um dispositivo médico e que as instruções de utilização e outra documentação fornecida pelo fabricante devem conter detalhes sobre a forma como o software e os acessórios apropriados devem ser selecionados.
Software: Refere-se a um conjunto de instruções que processa dados de entrada e cria dados de saída.
Determinação de Software de Dispositivos Médicos
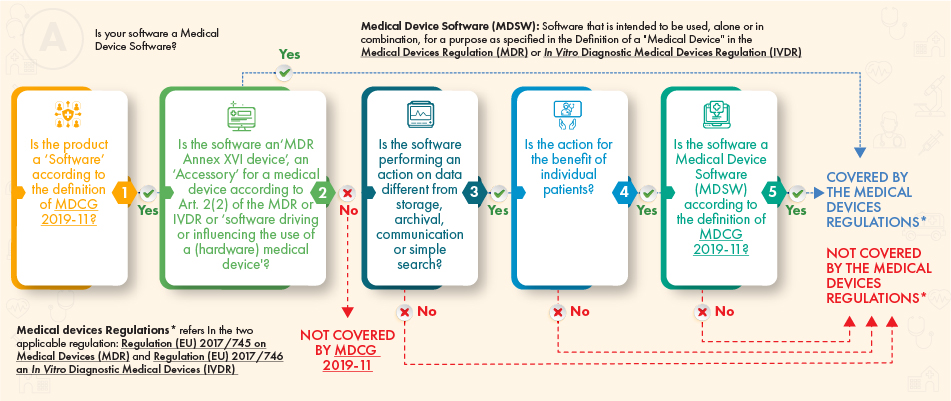
De acordo com o fluxograma da orientação acima, o software em questão deve estar sujeito a regulamentação, se cumprir os seguintes critérios:
- A definição de um dispositivo médico, um acessório do mesmo, ou impulsiona as operações do dispositivo médico, ou
- Realiza processamento adicional de dados (não apenas armazenamento ou comunicação) e a sua ação cria benefícios para os pacientes e cumpre a definição de software de dispositivo médico de acordo com a orientação MDCG
Determinação de Software de Dispositivos Médicos para Diagnóstico In Vitro
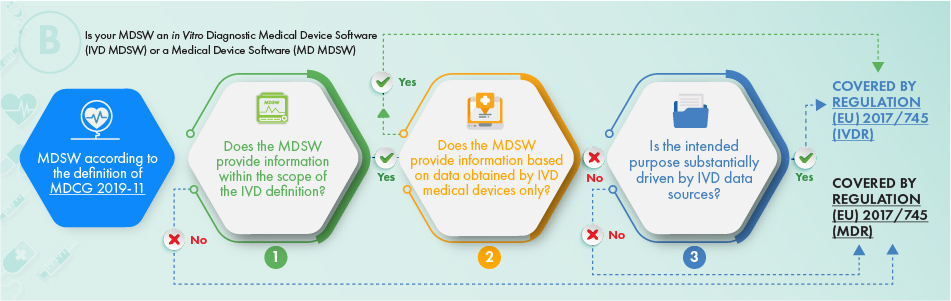
O fluxograma acima descreve a abordagem a ser aplicada, no que diz respeito aos produtos destinados a fins de diagnóstico in vitro. Para determinar se o software em questão deve estar sujeito a regulamentação, os seguintes critérios devem ser considerados:
- A definição de um dispositivo médico, um acessório do mesmo, ou impulsiona as operações do dispositivo médico, ou
- Fornece as informações normalmente fornecidas por dispositivos médicos para diagnóstico in vitro e apenas as informações recolhidas de um dispositivo médico para diagnóstico in vitro, ou
- A finalidade prevista do software está relacionada com questões do IVDR
De acordo com a orientação MDCG, o tipo de interconexão entre o software de dispositivo médico e o dispositivo não afeta a qualificação do software como dispositivo ao abrigo do MDR e do IVDR. Um software de dispositivo médico pode existir como um produto autónomo ou ser incorporado num dispositivo de hardware e esclarece os seguintes requisitos regulamentares:
- Considerando a sua qualificação e classificação, um produto de software de dispositivo médico autónomo deve ser submetido a todo o âmbito dos procedimentos regulamentares de acordo com a legislação aplicável.
- Um software de dispositivo médico que seja um componente integral ou parte de um dispositivo médico de hardware poderá ser colocado no mercado ao abrigo do procedimento simplificado. Seria sujeito a revisão não separadamente, mas durante a avaliação geral do próprio dispositivo médico de hardware.
Em resumo, a orientação do MDCG abrange os aspetos vitais relacionados com a classificação de software de dispositivos médicos e a determinação dos requisitos de regulamentação a serem aplicados. Os fabricantes de dispositivos médicos, desenvolvedores de software e outras partes devem seguir e implementar as recomendações do MDCG para garantir a conformidade. Para obter mais informações sobre como determinar o seu software como um dispositivo médico, consulte um especialista de regulamentação. Mantenha-se informado. Mantenha-se em conformidade.









