A aplicação de tecnologias de software na gestão de saúde, incluindo o diagnóstico ou tratamento de uma condição de doença, está a acelerar a um ritmo sem precedentes. As Autoridades globais de dispositivos médicos estão a rever os seus regulamentos e diretrizes para abordar estas tecnologias de dispositivos em crescimento. Na Austrália, a Therapeutic Goods Administration (TGA) é a Autoridade Reguladora responsável pela supervisão de dispositivos médicos, incluindo software e aplicações móveis. Em janeiro de 2021, a TGA publicou o rascunho original sobre os regulamentos de software para dispositivos médicos, que foi revisto em fevereiro de 2021. A 27 de julho de 2021, a TGA publicou um fluxograma detalhado que aborda as ambiguidades comuns que os fabricantes de dispositivos e os profissionais de regulamentação podem ter em relação à classificação de software para dispositivos médicos.
A TGA identifica o software utilizado no domínio dos dispositivos médicos como Software como Dispositivo Médico (SaMD), Software incorporado num dispositivo médico (SiMD) e Software que controla dispositivos médicos. De acordo com a TGA, o termo Software como Dispositivo Médico (ou SaMD) é qualquer software que pode funcionar num computador portátil, smartphone ou tablet cujo propósito pretendido se enquadra nas normas de um dispositivo médico. Em contraste, o SiMD é um software que é parte integrante de um dispositivo e é geralmente importante para o funcionamento preciso do dispositivo. Alguns softwares controlam os dispositivos médicos fisicamente ou através de ligações sem fios como Bluetooth, Wi-Fi, etc. A TGA regulamenta todos os três (03) tipos de software.
Poucos softwares de dispositivos médicos são excluídos ou isentos da regulamentação de software como dispositivo médico da TGA com base nos princípios de alinhamento da regulamentação com a regulamentação internacional e de redução do encargo através da não regulamentação dos produtos, onde não existe um risco significativo para a segurança, e onde já existem estruturas ou quadros adequados para os controlos do produto ou sistema.
| Dispositivos de Software Isentos | Dispositivos de Software Excluídos |
|---|---|
Ex.: Poucos sistemas de apoio à decisão clínica que cumprem três critérios principais: 1. Se o software não se destina a analisar ou processar uma imagem médica. 2. O software destina-se apenas a fornecer apoio/recomendação ao profissional de saúde. 3. O software não se destina a substituir o julgamento clínico do profissional. | Os produtos que não se enquadram na categoria de dispositivos médicos e não estão sujeitos a quaisquer requisitos regulamentares da TGA são designados como dispositivos de software excluídos. Ex.:
|
A TGA reviu a regulamentação de dispositivos médicos que incluem software que controla ou interage com outros dispositivos médicos, seja externa ou internamente, e o software que funciona como um dispositivo médico (por si só). As principais alterações incluem a introdução de novas regras de classificação, esclarecendo o limite dos produtos de software regulamentados, e os princípios essenciais foram atualizados para clarificar os requisitos para dispositivos médicos baseados em software.
Com a introdução de novas regras de classificação, alguns dispositivos médicos baseados em software estão a ser reclassificados para classes de risco mais elevadas e devem ser submetidos a procedimentos de avaliação da conformidade relevantes. Os patrocinadores e fabricantes de tais dispositivos reclassificados devem ser listados no ARTG (Registo Australiano de Produtos Terapêuticos) antes de 25 de fevereiro de 2021. Os fabricantes e patrocinadores que já se candidataram à TGA antes de 25 de fevereiro de 2021, devem submeter um formulário de notificação à TGA.
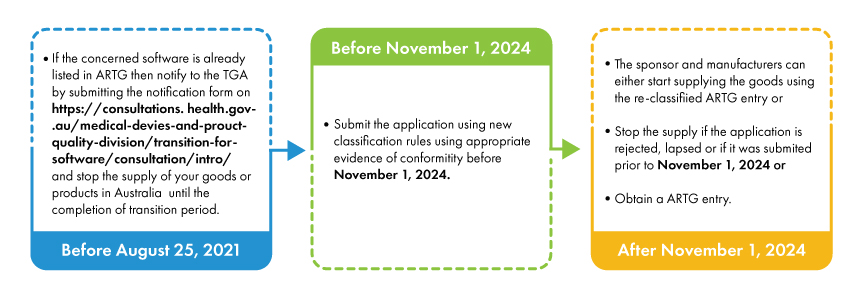
Classificação de software de dispositivos médicos na Austrália:
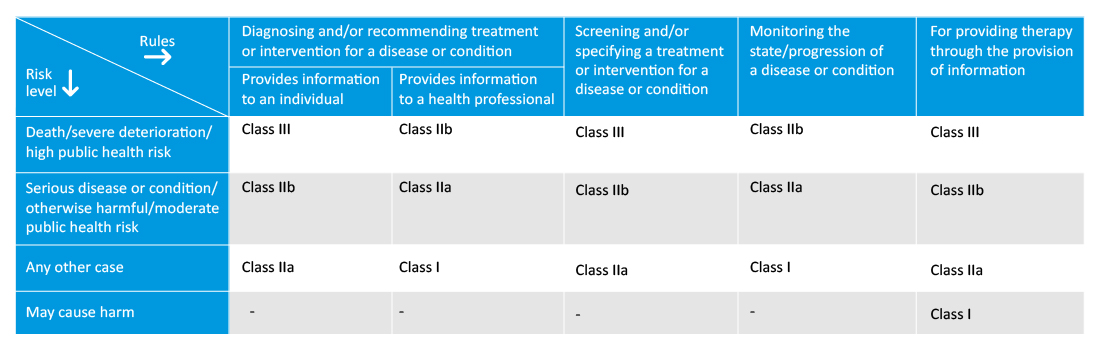
Os fabricantes devem especificar a finalidade pretendida do SaMD, o que ajudará na classificação e nos procedimentos de avaliação de conformidade. O novo regulamento também introduz as novas regras de classificação para dispositivos médicos programados e programáveis ou dispositivos médicos de software, e a classe do software dependerá da gravidade da doença monitorizada/tratada.
![]()
Alterações aos princípios essenciais:
Seguem-se as alterações efetuadas aos princípios essenciais com efeitos a partir de 25 de fevereiro de 2021, ao dispositivo médico baseado em software.
As alterações feitas nos regulamentos de software pela TGA podem aliviar o fardo do fabricante para categorizar o seu software como regulamentado ou não regulamentado e podem ajudar na preparação atempada dos documentos necessários para a avaliação de conformidade da TGA.
Com todos os cenários decifrados, pretende que o seu software seja listado no Registo Australiano de Produtos Terapêuticos (ARTG) com menos encargos? Para a listagem ARTG de dispositivos médicos, IVDs ou SaMDs, contacte um especialista. Mantenha-se informado. Mantenha-se em conformidade.