Submissões agendadas para 24 de setembro de 2016.
Agora que a segunda fase de conformidade UDI, para dispositivos médicos de Classe III I/LS/LS, foi implementada, muitos fabricantes de dispositivos, especialmente os do tipo Classe II, estão a questionar como podem melhor preparar-se para o prazo de submissão de dados de dispositivos de Classe II, a 24 de setembro de 2016. Para os alertar, na Freyr, identificámos alguns dos pré-requisitos que devem considerar para alinhar os dispositivos de Classe II com o mandato UDI da FDA.
A nova regulamentação exige que todos os dispositivos médicos de classe II sejam rotulados e embalados com um identificador único de dispositivo (UDI) e inseridos na Base de Dados Global de Identificação Única de Dispositivos (GUDID) da FDA. Dada a volatilidade dos requisitos de conformidade, juntamente com prazos de submissão mais curtos, o desafio para os fabricantes de dispositivos é conhecer os pormenores dos processos de conformidade. Ao mesmo tempo, devem garantir que nenhum dos principais atributos do dispositivo seja omitido ao reunir os dados dispersos do dispositivo em diferentes sistemas e ao reconciliá-los em folhas de cálculo para criar relatórios de conformidade.
Para ajudar os fabricantes de dispositivos a navegar facilmente por este processo de conformidade complexo e sensível ao tempo, sem erros, a Freyr compilou os seguintes pré-requisitos a serem seguidos.
Determinar a Data de Conformidade UDI: Desde que a FDA emitiu a sua regra final, algumas das datas de conformidade dos dispositivos foram alteradas e estendidas. Para planear meticulosamente as estratégias e processos de conformidade e para evitar alterações apressadas de última hora, os rotuladores devem determinar a data de conformidade precisa.
Data de Conformidade para Dispositivos de Classe II Requisitos de Conformidade 24 de Set de 2016Os dispositivos de Classe III que exigem rotulagem com um UDI devem apresentar um UDI como marcação permanente no próprio dispositivo, se o dispositivo for destinado a ser utilizado mais de uma vez e a ser reprocessado antes de cada utilização. Os rótulos e embalagens de dispositivos médicos de classe II devem conter um UDI As datas nos rótulos destes dispositivos devem ser formatadas conforme exigido O software autónomo de Classe II deve fornecer o seu UDI conforme exigido. Dados para dispositivos de classe II que devem ser rotulados com um UDI devem ser submetidos à base de dados GUDID Para a maioria dos dispositivos, a data de conformidade para a marcação direta é diferente dos outros requisitos. Com base na sua categoria de produto, quer seja destinado a ser reutilizado ou reprocessado, determine a data de conformidade UDI de marcação direta, conforme aqui apresentado:
Datas de Conformidade da Marcação Direta Categoria de Dispositivo – Reutilizado e Reprocessado 24 de Set de 2015 Dispositivos de suporte e manutenção da vida, independentemente da classe do dispositivo. 24 de Set de 2016 Dispositivos de Classe III e dispositivos licenciados ao abrigo da Lei do Serviço de Saúde Pública 24 de Set de 2018 Dispositivos da Classe II 24 de Set de 2020 Dispositivos de Classe I e dispositivos não classificados Avaliar a necessidade de Marcação Direta do número UDI: Todos os dispositivos médicos que são utilizados mais de uma vez ou que devem ser reprocessados antes de cada utilização devem ter marcação direta do UDI. A exceção é para dispositivos implantáveis que não exigem marcação direta de acordo com a regra UDI. Os dispositivos de uso único, mesmo que reprocessados, também não são obrigados a ter um UDI permanente – 21 CFR 801.45(d)(3). Assim, avalie a necessidade de Marcação Direta com base na categoria de dispositivos médicos que fabrica.
- Plano para Conformidade Abrangente: Analise os requisitos da FDA para os seus produtos específicos a serem cumpridos. Realize uma análise de lacunas completa para identificar deficiências relacionadas com dados ou tecnologia, a fim de lidar com alguns dos principais desafios no processo de cumprimento dos prazos rigorosos da FDA. Alguns dos desafios podem ser a obtenção de informações DI ou PI e o tratamento de grandes volumes de dados não estruturados de fontes díspares, etc. Em vez de trabalhar arduamente para reconciliar todos os dados de dispositivos médicos à última hora, planeie uma conformidade abrangente com antecedência através de sistemas e ferramentas validados que suportam a integração, qualidade e gestão de dados.
![]()
Obter número DI e Adesão à Agência: O UDI é composto pelo Identificador de Dispositivo (DI – número único baseado na versão ou modelo do dispositivo) e pelo Identificador de Produto (PI – inclui número de lote, número de série ou data de validade). A parte DI do UDI servirá como chave primária para procurar informações sobre o dispositivo na GUDID. Para atribuir o DI, a FDA acreditou três Agências Emissoras – GS1, HIBCC e ICCBBA. Neste cenário, os rotuladores devem obter a adesão a uma das agências para obter o número DI que precisa de ser introduzido na GUDID da FDA.
![]()
Identificador Atributos Agências Emissoras UDI DI (Identificador de Dispositivo – Dados Estáticos)
Requer sincronização com a GUDIDNúmero Único de
Fabricante
Marca do Dispositivo
Modelo do Dispositivo
GSI
HIBCC
ICCBBAPI (Identificador do Produto – Dados Dinâmicos)
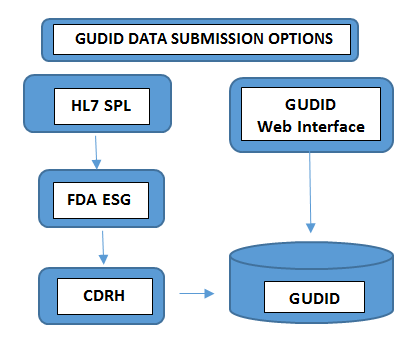
Obrigatório em todos os níveis de embalagemNúmero de Lote, Número de Série, Data de Fabrico, Data de Validade, - Submeter os Dados: A forma como submete os dados ao GUDID varia com o volume de portefólios de produtos que gere. Os fabricantes de dispositivos com um número mínimo de dispositivos optam por submeter as informações UDI manualmente através da interface web gratuita do GUDID da FDA. Neste caso, apenas um registo DI pode ser submetido de cada vez através de uma interface web GUDID segura. No outro caso, os fabricantes com um maior número de portefólios de produtos escolhem a opção de submissão HL7 SPL para recolher dados eletronicamente e converter os dados consolidados para o formato SPL antes de os submeterem ao Electronic Submission Gateway (ESG) da FDA, utilizando o número DUNS. Tenha em atenção que a conta GUDID não é por tipo de submissão. A conta serve para o identificar, o rotulador, para permitir a submissão de dados de dispositivos através de ambas as opções.
![]()
- Configurar uma Conta GUDID: Um rotulador / fabricante de dispositivos requer uma ou mais contas GUDID com base no número de funções a serem atribuídas; para citar algumas, coordenador GUDID, Utilizador de Entrada de Dados, etc. Mas para autorizar cada função para entrada de dados, o fabricante necessita de uma aprovação da FDA antes da criação da conta. O processo de criação de uma conta GUDID apropriada envolve o envio de um pedido por e-mail à FDA, após o qual o requerente, você, receberá um documento de pedido de conta para preencher. Assim que enviar o documento preenchido de volta à FDA por e-mail, a agência irá rever o formulário e, em seguida, enviar um e-mail com as informações de login da conta GUDID.
A implementação do UDI é um processo complexo e moroso. Ao longo do processo, e para cumprir os requisitos de UDI da FDA, os fabricantes de dispositivos médicos enfrentam muitos desafios relacionados com a gestão, integração e submissão de dados. Com o prazo de conformidade para dispositivos de Classe II a apenas um ano de distância, a Freyr recomenda que as empresas comecem a trabalhar nisso agora mesmo.
Para orientar a sua organização através deste complexo processo de conformidade, a Freyr oferece o melhor dos dois mundos – uma solução de software UDI a pedido, totalmente configurável, Freyr IDENTITY, bem como um Centro de Excelência (CoE) que oferece os melhores serviços UDI da sua classe, económicos e personalizáveis, serviços UDI construídos em torno das suas necessidades únicas e exigentes.