Um “dispositivo de referência” é um dispositivo médico que foi previamente aprovado pela US Food and Drug Administration (US FDA) e já se encontra no mercado, servindo como ponto de referência para novos dispositivos médicos que procuram aprovação através da via de autorização 510(k) da FDA.
O dispositivo em questão deve provar ser, pelo menos, tão seguro e eficaz quanto o dispositivo de referência em termos da sua utilização pretendida e características tecnológicas. Esta comparação é conhecida como determinação de “equivalência substancial”.
Um novo dispositivo não precisa de ser idêntico ao dispositivo de referência para ser substancialmente equivalente ao dispositivo de referência.
Como Identificar um Dispositivo Predicado?
A base de dados da FDA fornece um código de produto de três letras para cada classificação de dispositivo. A base de dados FDA 510(k) contém informações sobre todos os dispositivos aprovados através do processo 510(k). Uma vez que tenha o código de produto de três letras, pode obter uma lista de cada produto, cada empresa e o nome comercial de cada concorrente ou potencial concorrente que pretenda analisar. Pode então fazer uma análise e comparação aprofundadas para restringir a escolha de um dispositivo precedente.
Abaixo encontra-se um fluxograma que descreve o processo de identificação e seleção de um dispositivo precedente.
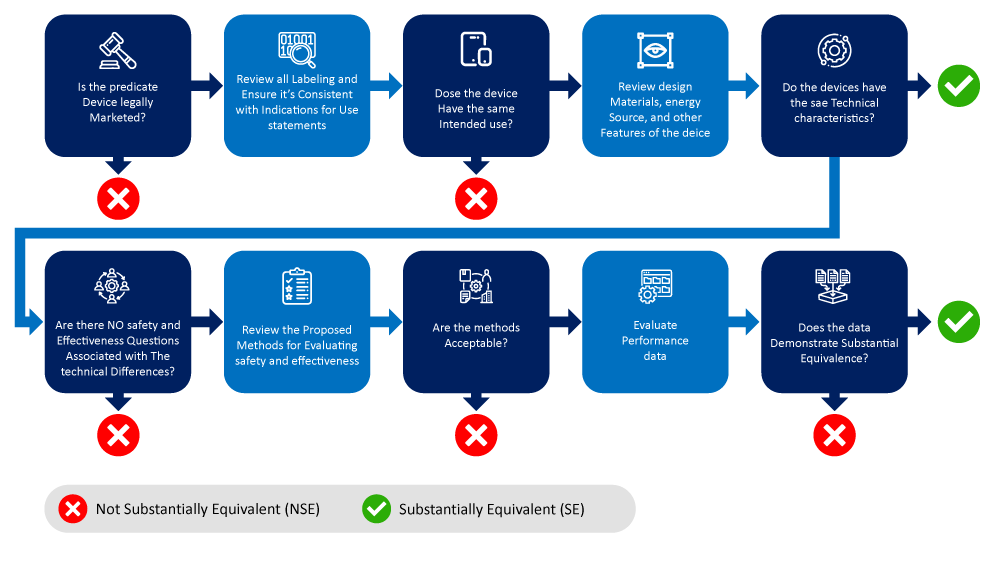
Fatores a Considerar ao Determinar o(s) Dispositivo(s) Predicado(s)
- Finalidade de utilização: A finalidade de utilização após o dispositivo de referência deve ser semelhante à do novo dispositivo. Por exemplo, se o novo dispositivo se destina a ser utilizado para monitorização cardíaca, o dispositivo de referência também deve ser um dispositivo de monitorização cardíaca.
- Características tecnológicas: O dispositivo precedente deve ser idêntico ao novo dispositivo em termos de características tecnológicas. Por exemplo, o design, os materiais utilizados e o método de operação devem ser semelhantes.
- Biocompatibilidade: As avaliações de biocompatibilidade de um dispositivo médico ou componente não devem limitar-se às matérias-primas utilizadas no dispositivo e no processo de fabrico, devendo também ser considerados produtos químicos adicionais. Este fator, no entanto, não se aplica aos IVD.
- Tecnologia mais recente: O dispositivo de referência não deve estar desatualizado e deve representar a mais recente tecnologia médica.
O dispositivo de referência é um fator chave para determinar se um novo dispositivo médico pode ser colocado no mercado através da via 510(k). Escolher o dispositivo de referência errado pode resultar num processo de aprovação regulamentar mais dispendioso e demorado, enquanto escolher o dispositivo de referência certo pode ajudar a reduzir o custo e o tempo necessários para colocar um novo dispositivo médico no mercado. Se o dispositivo de referência não for adequado, pode resultar em atrasos e despesas adicionais.
Para assistência com o processo de submissão 510(k) do seu dispositivo médico, agende uma chamada com os especialistas regulamentares da Freyr, que o podem ajudar a navegar pelos procedimentos. Mantenha-se informado. Mantenha-se em conformidade.









