
O 510(k) é uma submissão pré-comercialização feita à FDA para demonstrar que o dispositivo a ser comercializado é tão seguro e eficaz, ou seja, substancialmente equivalente a um dispositivo legalmente comercializado (predicado). Os dispositivos com risco moderado são obrigados a submeter uma notificação 510(k), que inclui uma minoria de dispositivos de Classe I e III e a maioria dos dispositivos de Classe II.
Existem três (03) tipos de programas 510(k): Tradicional, Abreviado e Especial. A via de segurança e desempenho foi introduzida em 2019 e baseou-se no programa abreviado. O programa eSTAR, introduzido em 2020, permite a submissão abrangente de dispositivos médicos através de um formulário PDF interativo.
Quem Precisa de uma Certificação 510(k)?
510(k) é essencialmente o nome do processo/via a que os fabricantes de dispositivos médicos que pretendem comercializar os seus dispositivos de risco moderado a elevado nos US se submetem para demonstrar que o produto a ser comercializado é tão seguro e eficaz quanto um dispositivo legalmente comercializado.
Detalhado abaixo está o processo passo a passo para a obtenção de uma autorização 510(k).
Passo 1 – Identificação do Código de Classe do Dispositivo, Tipo de Submissão e Dispositivo Predicado
- Identificar o código do produto e o número de regulamentação- Para determinar os requisitos de teste 510(k), é necessário primeiro identificar o código do produto e o número de regulamentação. Pode-se iniciar uma pesquisa na base de dados da FDA para encontrar o número de regulamentação de 7 dígitos cuja identificação corresponde ao uso pretendido do dispositivo em questão.
- O código de produto da FDA consiste em três (03) letras. Informações sobre a classificação do produto, descrição da regulamentação e requisitos de BPF podem ser localizadas utilizando este código.
- Seleção do tipo de submissão - Um requerente pode escolher um dos três (03) tipos de submissão mencionados anteriormente. O 510(k) Tradicional é para submissões iniciais, o 510(k) Especial é para fabricantes de dispositivos médicos que desejam submeter alterações a um dispositivo existente e o 510(k) Abreviado pode ser escolhido quando o dispositivo cumpre as normas de consenso voluntário estabelecidas. No caso de um 510(k) Abreviado, o requerente deve basear-se nos documentos de orientação da FDA.
- Identificação do dispositivo de referência - Um fabricante de dispositivos médicos precisa de provar que o dispositivo que pretende comercializar tem a mesma finalidade de utilização e características técnicas que o dispositivo legalmente comercializado, também conhecido como dispositivo de referência. Se existirem diferenças nas características técnicas, o requerente deve provar que não existem preocupações de segurança e eficácia associadas a essa diferença.
Passo 2 – Preparação do Processo 510(k)
O próximo passo é preparar o ficheiro 510(k), a orientação e a informação, que está disponível no website da FDA. Inclui a lista de verificação de aceitação para todos os três (03) tipos de programas 510(k) e um microsite intitulado Content for 510(k), que inclui informações relativas a declarações para indicações de uso, comparação de equivalência substancial e rotulagem proposta, entre outras informações úteis.
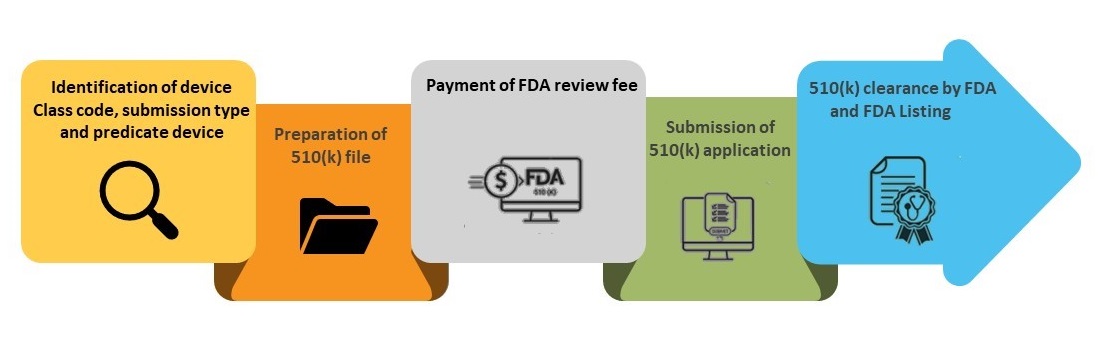
etapas do processo de submissão 510(k)
Passo 3 - Pagamento da Taxa de Revisão da FDA
Todos os tipos de submissões 510(k) estão sujeitos à taxa de utilizador. Para o ano financeiro de 2023, a taxa padrão para 510(k) é de $19 870. Para empresas certificadas pelo Centre for Diagnostics and Radiological Health (CDRH), também conhecidas como pequenas empresas, a taxa é de $4 967. A taxa está sujeita a alterações no próximo ano financeiro.
Passo 4 - Submissão 510(k)
O requerente pode enviar uma cópia eletrónica (eCopy) ou uma submissão pré-comercialização através do Modelo e Recurso de Submissão Eletrónica (eSTAR) pelo portal CDRH.
A partir de 1 de outubro de 2023, todas as submissões 510(k), salvo isenção de acordo com a orientação final, devem ser submetidas como submissões eletrónicas utilizando o eSTAR.
Após a submissão do 510(k), é atribuído um número de controlo único, conhecido como o “número 510(k)” ou “número K”. A FDA realiza duas verificações: uma para verificar se a taxa de utilizador adequada foi paga e a segunda para verificar se foi fornecido um eCopy ou eSTAR válido.
- Até ao 7.º dia, a FDA envia uma carta de confirmação caso a taxa de utilizador adequada seja paga e seja fornecida uma eCopy ou eSTAR válida. Caso contrário, a FDA envia uma carta de suspensão para questões não resolvidas.
- Até ao 15.º dia, a FDA realiza uma revisão de aceitação. A FDA informa o requerente se o 510(k) é aceite para revisão substantiva ou se é colocado em suspensão por Recusa de Aceitação (RTA).
- Até ao 60.º dia, a FDA realiza uma revisão substantiva. A FDA comunica através de
interação substantiva para informar que irá prosseguir com uma revisão interativa, ou que o 510(k) será colocado em suspensão e serão solicitadas Informações Adicionais.
Passo 5 - Aprovação da FDA e Inscrição na Base de Dados 510(k) da FDA
O objetivo da FDA é anunciar a sua decisão sobre as Alterações à Taxa de Utilizador de Dispositivos Médicos (MDUFA) em 90 dias FDA. Os dias FDA são os dias de calendário entre a data de receção do 510(k) e a data de uma decisão MDUFA, excluindo os dias em que a submissão esteve suspensa devido a um pedido de informações adicionais. As decisões MDUFA para submissões 510(k) incluem conclusões de substancialmente equivalente (SE) ou não substancialmente equivalente (NSE).
Quando uma decisão é tomada, a FDA emite uma carta de decisão ao requerente por e-mail. Uma submissão 510(k) que recebe uma carta de decisão SE é considerada “aprovada.” É então listada na base de dados 510(k) juntamente com as Indicações de utilização do dispositivo médico e o resumo 510(k) ou a declaração 510(k) como anexos.
Pode-se concluir que um planeamento e uma execução cuidadosos, através de documentação exaustiva e de uma compreensão aprofundada do ambiente regulamentar, são cruciais para uma submissão 510(k) bem-sucedida à FDA.
Para assistência com o processo de submissão 510(k) do seu dispositivo médico, pode escrever-nos para sales@freyrsoltions.com, ou agendar uma chamada com os nossos especialistas, que o podem ajudar a navegar pelos procedimentos. Mantenha-se informado. Mantenha-se em conformidade.









