A nível mundial, as agências de saúde exigem que os fabricantes estrangeiros de dispositivos médicos e de diagnóstico in vitro nomeiem um representante local. No Japão, ao abrigo da Lei revista sobre Produtos Farmacêuticos e Dispositivos Médicos (PMD), o sistema de «In-Country Caretaker» (ICC) foi substituído pelo sistema Autorização de Introdução no Mercado (MAH). Ao abrigo deste sistema, as empresas devem obter uma MAH para obter a aprovação dos dispositivos e comercializá-los no Japão.
Autorização de Introdução no Mercado (MAH) deve ser uma entidade local sediada no Japão. Os fabricantes nacionais podem obter diretamente a MAH , enquanto os fabricantes estrangeiros devem designar uma entidade local para cumprir este MAH de MAH .
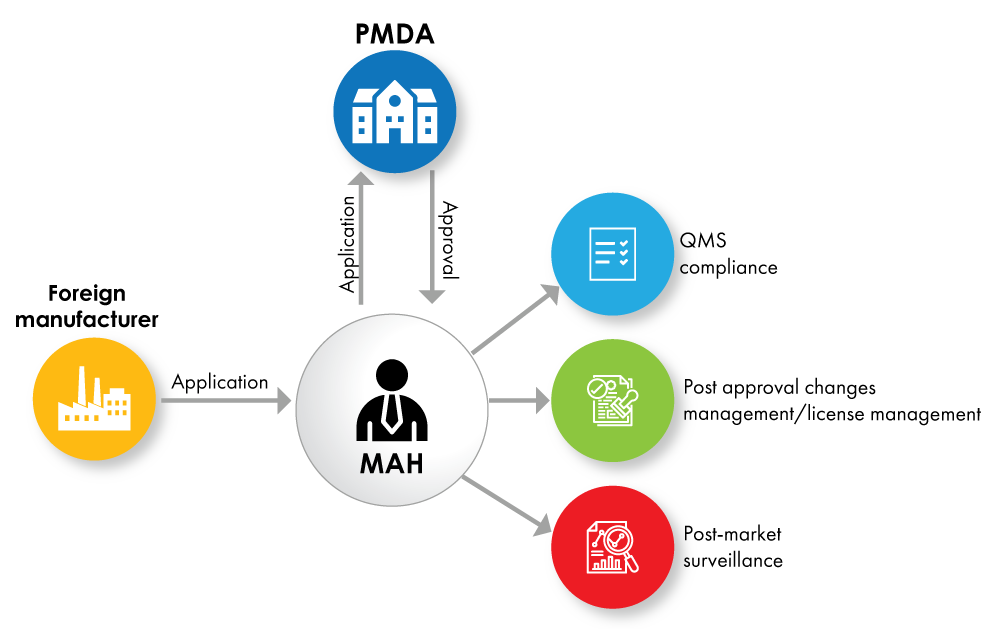
Fig. n.º 1: Fluxograma do registo de dispositivos com MAH titular da licença
Se os fabricantes estrangeiros não desejarem ceder a titularidade total do produto ao MAH Autorização de Introdução no Mercado MAH, podem nomear um Autorização de Introdução no Mercado Designado Autorização de Introdução no Mercado (DMAH). O DMAH apresenta o submissão nome do fabricante estrangeiro, e a aprovação é concedida ao fabricante estrangeiro para o dispositivo.
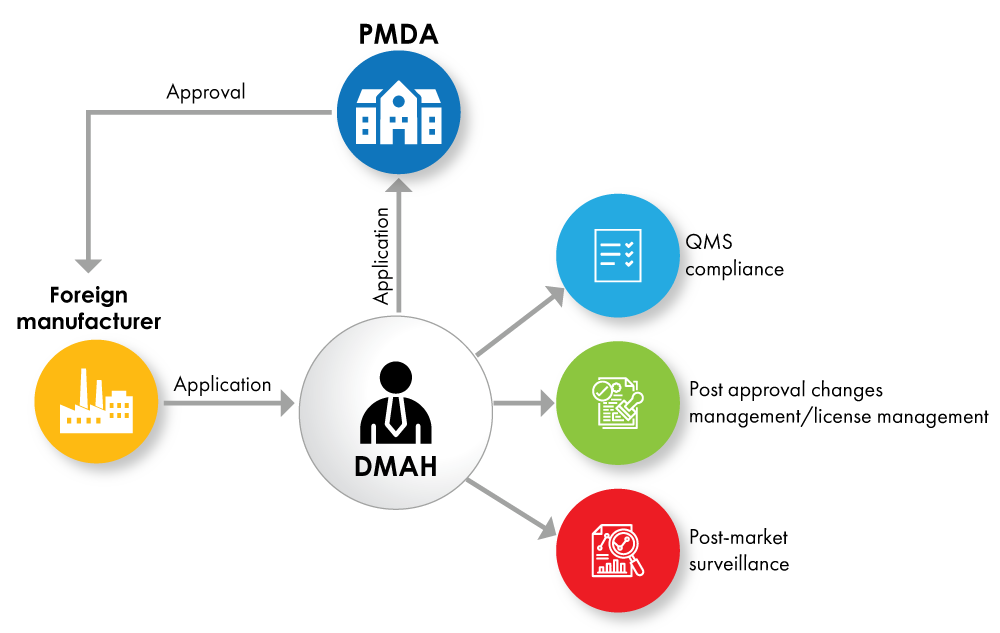
Fig. N.º 2: Fluxograma de Registo de Dispositivo com o DMAH como Titular da Licença
Existem três (03) opções possíveis através das quais o fabricante estrangeiro pode cumprir o MAH PMDA MAH . Os fabricantes estrangeiros devem avaliar minuciosamente todas as três (03) possibilidades. Estas incluem:
Estabelecer uma Filial no Japão
Os fabricantes estrangeiros podem abrir um escritório local no Japão e atuar como titulares MAH lançar os seus produtos no Japão. Isto permite que o fabricante estrangeiro tenha total controlo e visibilidade sobre os seus produtos no Japão. Esta opção pode não ser a preferida para fabricantes de pequena dimensão, uma vez que os custos associados à criação de uma filial no Japão e ao cumprimento dos requisitos de qualidade do Ministério da Saúde, do Trabalho e do Bem-Estar ( MHLW) são bastante elevados.
Distribuidor na qualidade de MAH da MAH de MAH no mercado
Trata-se de uma opção económica para os fabricantes estrangeiros que não possuem um escritório local no Japão. Os importadores ou distribuidores podem ser nomeados como MAH DMAH. Tendo em conta as receitas geradas pela venda dos dispositivos, os importadores e distribuidores geralmente não cobram taxas adicionais para atuarem como MAH DMAH. Os fabricantes, no entanto, enfrentam desafios na penetração no mercado, uma vez que o distribuidor que atua como MAH não estar disposto a emitir um Certificado de Não Objeção (NoC) a outros distribuidores. Por vezes, os distribuidores não cooperam com o fabricante estrangeiro na mudança do MAH na transferência da licença do dispositivo para o MAH recém-identificado.
Aliança com Terceiros
Os fabricantes estrangeiros podem nomear um prestador de serviços independente como seu MAH. A confidencialidade do dispositivo é rigorosamente salvaguardada e o fabricante estrangeiro mantém o controlo da propriedade legal do produto. Os fabricantes podem implementar e concretizar os seus planos de expansão de mercado.
Responsabilidades do Titular de Autorização de Introdução no Mercado
Um MAH atua como representante do fabricante estrangeiro e presta assistência no processo de aprovação de dispositivos no Japão. As principais responsabilidades de um MAH incluem:
- End-to-end aprovação de dispositivos
- Garantir que dispositivos seguros e de qualidade entrem no mercado japonês através da gestão adequada do fabrico e controlo de qualidade dos produtos.
- Ser responsável pela libertação do dispositivo à parte que possui uma licença de venda/distribuição de dispositivos médicos
- Gestão das atividades de Vigilância Pós-Comercialização (PMS)
Uma vez que o MAH deve cumprir todas as medidas de segurança, do Sistema de Gestão da Qualidade (SGQ) e das Boas Práticas de Vigilância (BPV) em nome do fabricante estrangeiro, é extremamente importante escolher o MAH adequado. Por conseguinte, os fabricantes estrangeiros devem avaliar minuciosamente todas as opções antes de optar pelo melhor MAH possível. Estas incluem a realização de uma análise de viabilidade, a determinação do RoI, a relação com os importadores e distribuidores, o orçamento disponível, a dimensão do portfólio, o lucro com as vendas do dispositivo, os prazos para o lançamento do dispositivo, etc. Os fabricantes devem escolher meticulosamente se atribuem a titularidade do dispositivo ao MAH se nomeiam um DMAH e mantêm a titularidade consigo.
Para saber mais sobre os requisitos relativos MAH no Japão, reach um especialista em regulamentação da Freyr. Mantenha-se informado. Mantenha-se em conformidade.









