
Os dispositivos médicos são submetidos a avaliação da conformidade antes de serem incluídos na lista ARTG para garantir que os dispositivos cumprem os princípios essenciais exigidos pela Therapeutic Goods Administration (TGA), Austrália. Os princípios essenciais descrevem basicamente as características de segurança e desempenho que qualquer dispositivo deve cumprir, para que possa ser vendido na Austrália. Semelhante ao processo na UE, a avaliação da conformidade na Austrália baseia-se na classe de risco do dispositivo. Portanto, a via de avaliação da conformidade a ser seguida por qualquer dispositivo depende da sua classificação.
Existem várias normas regulatórias que se aplicam a vários tipos de dispositivos. O cumprimento de uma ou mais das normas é exigido como um requisito essencial. A identificação das normas relevantes aplicáveis ao dispositivo e os testes subsequentes do dispositivo para demonstrar a sua conformidade com a norma tornam-se um pré-requisito.
A avaliação da conformidade envolve um exame sistemático dos documentos técnicos relacionados com o dispositivo. A gestão de riscos, a avaliação clínica, o processo de fabrico envolvido e as atividades de vigilância geridas pelo fabricante são as áreas críticas para avaliação. Os dispositivos que são obrigados a ter um certificado de Avaliação de Conformidade da TGA estão listados no Regulamento 4.1 do Therapeutic Goods (Medical Devices) Regulations 2002. Embora um certificado de avaliação da conformidade emitido pela TGA seja um pré-requisito para a comercialização da maioria dos dispositivos médicos na Austrália, a TGA também aceita certificados de avaliação da conformidade emitidos pelos Organismos Notificados na Europa. Além disso, a TGA também aceita a avaliação da conformidade de países que fazem parte do MDSAP (Medical Device Single Audit Program).
Os requisitos de avaliação da conformidade variam com a categoria de risco do dispositivo. A Tabela n.º 1 detalha o processo de avaliação da conformidade baseado na classificação na Austrália.
Processo de Avaliação da Conformidade - Austrália
Classe | Procedimento de Avaliação da Conformidade | Responsabilidades do Fabricante |
| I | Parte 6 (Declaração de Conformidade, não exigindo avaliação pelo Secretário) | Documentação para demonstrar conformidade com os Princípios Essenciais |
| I (medição) e IIa (não estéril) | Parte 6 (Declaração de Conformidade, não exigindo avaliação pelo Secretário) Parte 5 (Sistema de gestão da qualidade do produto) | Documentação para demonstrar conformidade com os Princípios Essenciais. Implementar um sistema de gestão da qualidade do produto para inspeção e testes finais para auditorias. Nota: A apresentação da Declaração de Conformidade não é exigida para a Classe I (não-medidora e não estéril), mas deve estar disponível a pedido da TGA. |
| I (estéril) & IIa (estéril) | Parte 6 (Declaração de Conformidade, não exigindo avaliação pelo Secretário) Parte 4 (Garantia de Qualidade da Produção) | Documentação para demonstrar conformidade com os Princípios Essenciais. Implementar um sistema de gestão da qualidade que exclui o elemento de conceção, com base na ISO 13485. |
| IIb | Parte 1 (Garantia de Qualidade Total) excluindo a Cláusula 1.6 (Exame do projeto) | Implementar um sistema de gestão da qualidade completo, incluindo conceção, produção, rotulagem, embalagem e inspeção final, com base na ISO 13485. Exclui o dossier de conceção. |
| III & AIMD | Parte 1 (Garantia de Qualidade Total) incluindo a Cláusula 1.6 (Exame do projeto) | Implementar um sistema de gestão da qualidade completo, incluindo conceção, produção, rotulagem, embalagem e inspeção final, com base na ISO 13485. Dossiê de conceção em conformidade com os Princípios Essenciais. |
| Sistemas ou Conjuntos de Procedimentos Parte 7 | (Procedimentos para Dispositivos Médicos Utilizados para um Fim Específico) | Princípios Essenciais. Procedimento de Avaliação da Conformidade. Evidência clínica para componente individual em sistema ou embalagem. |
Tabela N.º 1. Requisitos de Avaliação da Conformidade dos Dispositivos
O processo de aprovação habitual de dispositivos médicos pela TGA é o seguinte:
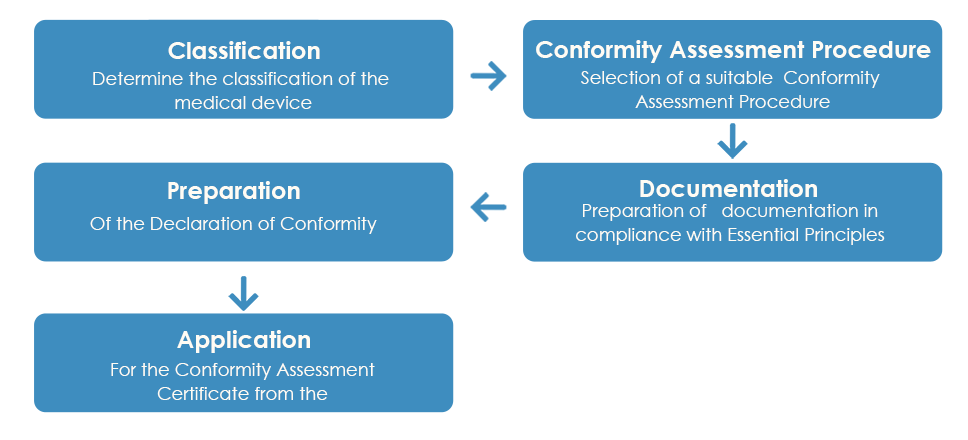
Conforme detalhado acima, uma vez recebido o Certificado de Avaliação da Conformidade da TGA, uma Declaração de Conformidade (DoC) precisa de ser preparada pelo fabricante, declarando que o dispositivo médico cumpre os princípios essenciais aplicáveis, as regras de classificação e a via de avaliação da conformidade. No entanto, ao contrário do Certificado de Avaliação da Conformidade, uma DoC europeia não é aceite pela TGA.
O mercado australiano oferece um panorama promissor para fabricantes de dispositivos médicos, desde que os requisitos regulamentares da Therapeutic Goods Administration (TGA) sejam cumpridos. Os requisitos de conformidade e o processo de avaliação variam com a classe de risco do dispositivo e do IVD. Embora os regulamentos de dispositivos médicos sejam bem definidos e transparentes, navegar por eles é complexo e os fabricantes podem procurar apoio junto de parceiros de regulamentação para o registo bem-sucedido do dispositivo.
Para obter informações abrangentes sobre os requisitos de avaliação da conformidade, o Patrocinador Australiano e a listagem ARTG na Austrália, para mais informações, contacte um especialista Regulamentar comprovado. Mantenha-se informado. Mantenha-se em conformidade.









