
O Regulamento de Dispositivos Médicos (MDR) da União Europeia (UE) tem sido notícia há já algum tempo. O MDR substituiu a Diretiva de Dispositivos Médicos (MDD) e a Diretiva de Dispositivos Médicos Ativos Implantáveis (AIMDD). Inicialmente, toda a transição estava prevista para entrar em vigor em maio de 2020; no entanto, devido ao surgimento da pandemia de COVID-19, a implementação foi adiada para 26 de maio de 2021. Neste cronograma, até 26 de maio de 2024, todos os certificados MDD tornar-se-ão nulos, e os fabricantes de dispositivos serão obrigados a estar em conformidade com o EU MDR. Além disso, os dispositivos MDD legalmente colocados no mercado nos termos das Diretivas 90/385/CEE e 93/42/CEE antes de 26 de maio de 2020, e os dispositivos colocados no mercado a partir de 26 de maio de 2020, por força de um certificado, continuarão a ser disponibilizados no mercado até 27 de maio de 2025. Os prazos são apresentados abaixo –
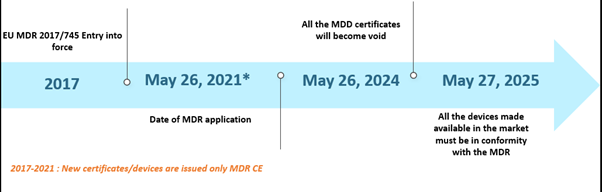
Prazos do Cenário Passado do EU MDR
No entanto, a capacidade limitada dos Organismos Notificados (ONs) e a falta de preparação dos fabricantes apresentaram alguns desafios na implementação do MDR de acordo com o prazo estabelecido. Em outubro de 2022, existiam, no total, trinta e oito (38) Organismos Notificados (ONs), e estes ONs receberam cerca de 8120 submissões para a certificação EU MDR, das quais foram emitidos 1990 certificados. De acordo com as suas estimativas e o prazo inicial, apenas 7000 certificados poderiam ser processados, o que levou à extensão do prazo. Além disso, uma das outras prováveis razões para a extensão foi garantir a disponibilidade contínua de dispositivos médicos seguros cujos certificados já expiraram ou estão prestes a expirar antes de 26 de maio de 2024. O cenário atual para o prazo estendido é apresentado abaixo-
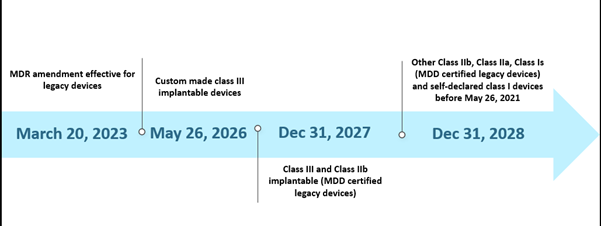
Prazos do Cenário Passado do EU MDR
A nova extensão é aplicável a dispositivos legados que cumprem o artigo 120 (3e) com uma marcação CE MDD válida ou derrogação a 20 de março de 2023, e permanecerá no mercado juntamente com os dispositivos com marcação CE MDR. Até 26 de maio de 2024, os fabricantes de dispositivos legados devem ter um QMS implementado e ter apresentado uma submissão a um NB designado pela MDR para avaliação da conformidade, e até 26 de setembro de 2024, os fabricantes de dispositivos legados devem ter um acordo com um NB designado pela MDR.
Vejamos agora o impacto que os fabricantes poderão ter com esta extensão.
Oportunidades que os fabricantes têm com esta extensão:
- Acesso alargado ao mercado para os fabricantes de dispositivos certificados pela MDD/AIMDD que já tomaram iniciativas de conformidade com o MDR.
- Os fabricantes certificados pela MDR cujos certificados CE MDD/AIMDD não foram revogados têm permissão para colocar dispositivos legados no mercado até ao final do período de transição, para além dos seus dispositivos em conformidade com a MDR.
- Os fabricantes que têm uma derrogação nacional a partir de 20 de março de 2023 podem beneficiar do período de transição.
- O período de extensão concede mais tempo para uma melhor compreensão das regras e regulamentações, o que ajuda a otimizar o processo e a alcançar a conformidade com o MDR.
Desafios que podem surgir para os fabricantes com esta extensão:
- Não há benefício de mercado para os fabricantes de dispositivos legados que não quiseram cumprir o MDR.
- A extensão da MDR pode fazer com que os processos de certificação se prolonguem e atrasem os lançamentos de produtos, o que é um resultado direto do atraso nas revisões pelos Organismos Notificados.
Que ações devem os fabricantes tomar?
- É imperativo que os fabricantes determinem a classe de risco MDR do seu dispositivo médico para identificar prontamente o cronograma de transição apropriado de acordo com os regulamentos MDR alterados.
- Para garantir a conformidade com os regulamentos MDR, é crucial identificar e iniciar a comunicação com os Organismos Notificados (ON) designados pela MDR que possuam a competência específica exigida para a classificação do seu dispositivo médico.
- É fundamental realizar uma avaliação abrangente de lacunas para o seu dispositivo médico certificado ao abrigo da MDD/AIMDD, identificar e abordar quaisquer não conformidades com os regulamentos MDR e garantir a conformidade atempada.
É essencial que os fabricantes tomem medidas imediatas para garantir a conformidade com o MDR. O prazo alargado oferece algumas oportunidades para os fabricantes alcançarem a conformidade com o MDR, mas também apresenta desafios, como processos de certificação atrasados e o custo da conformidade. Para superar estes desafios e capitalizar as oportunidades, deixe a nossa equipa de profissionais ajudá-lo no processo de conformidade com o MDR e garantir o seu sucesso neste desafiante ambiente regulamentar. Marque uma consulta connosco hoje para saber mais sobre como podemos ajudá-lo a alcançar a conformidade com o MDR e a manter-se à frente da concorrência. Mantenha-se informado. Mantenha-se em conformidade.









