
Os dispositivos médicos desempenham um papel vital na melhoria da saúde do paciente, mas podem ocorrer não conformidades nos dispositivos, mesmo com os melhores sistemas de controlo de qualidade em vigor. Não conformidades referem-se a situações em que um produto ou processo não cumpre os requisitos regulamentares, as normas de qualidade ou os procedimentos internos aprovados. Uma gestão eficaz das não conformidades é importante para garantir a segurança do paciente, a conformidade regulamentar e a reputação dos fabricantes de dispositivos médicos.
Este blog explora a importância da gestão de não conformidades em dispositivos médicos, o processo e as melhores práticas.
A Importância da Gestão de Não Conformidades em Dispositivos Médicos
Uma gestão eficaz de não conformidades pode ajudar a identificar potenciais problemas precocemente, prevenir danos aos pacientes e melhorar a qualidade geral dos dispositivos médicos. Pode também ajudar os fabricantes a cumprir os requisitos regulamentares, manter a satisfação do cliente e, em última análise, melhorar os resultados financeiros, reduzindo os custos e a mão de obra associados a falhas de produtos e recolhas.
Por outro lado, se as não conformidades não forem identificadas e abordadas prontamente, podem levar à falha do dispositivo, não conformidade regulamentar e podem ter efeitos prejudiciais na saúde do doente. Se um produto não conforme for lançado no mercado, pode resultar em recolhas dispendiosas, repercussões legais e danos à reputação do fabricante.
O Processo de Gestão de Não Conformidades em Dispositivos Médicos
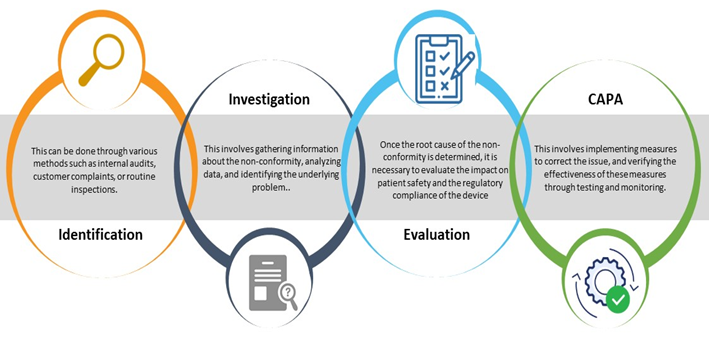
O processo de gestão de não conformidades em dispositivos médicos envolve várias etapas, incluindo identificação, investigação, Análise da Causa Raiz (RCA), avaliação de impacto e planeamento de Ações Corretivas e Preventivas (CAPA). O processo deve ser bem documentado com relatórios de não conformidade, e todas as partes interessadas devem ser formadas no processo para garantir a sua eficácia.
Cinco (05) Práticas Que Pode Adotar para uma Gestão Eficaz de Não Conformidades em Dispositivos Médicos
A gestão eficaz de não conformidades em dispositivos médicos requer uma abordagem sistemática e proativa para identificar e abordar não conformidades. Seguem-se algumas das melhores práticas para uma gestão eficaz de não conformidades em dispositivos médicos:
- Um Sistema de Gestão da Qualidade (QMS) Robusto-: Estabelecer e manter um QMS eficaz que inclua procedimentos para identificar e gerir não-conformidades.
Formação de Pessoal: Garantir que todo o pessoal é formado nos procedimentos de gestão de não conformidades, incluindo o processo de como identificar, investigar, avaliar, realizar uma avaliação de impacto e implementar CAPA.
- Manutenção de Registos: Manter todos os registos e documentar qualquer informação relacionada com o acompanhamento de não conformidades, RCA, avaliação de impacto e CAPA.
- Auditorias Internas Regulares: Realizar auditorias internas regularmente para avaliar a eficácia do processo de gestão de não conformidades e identificar áreas de melhoria.
Melhoria Contínua: Promover uma cultura de melhoria contínua, incentivando o feedback de todas as partes interessadas, incluindo clientes, fornecedores e colaboradores.
É crucial implementar uma gestão eficaz de não conformidades para garantir a segurança do paciente, a conformidade regulamentar e proteger a reputação dos fabricantes de dispositivos médicos. Pode conseguir isto criando um SGQ robusto que possa identificar e abordar com precisão as não conformidades, prevenindo, em última análise, a sua ocorrência e melhorando a qualidade geral dos dispositivos médicos. Crie um SGQ robusto para o seu dispositivo médico e garanta a sua conformidade e a segurança do paciente com a assistência dos nossos especialistas em regulamentação. Mantenha-se informado! Mantenha-se em conformidade!









