Serviços de Conformidade, Auditoria e Validação - Visão Geral
Está em conformidade? Esta é uma questão à qual qualquer empresa dos setores farmacêutico, biotecnológico, genómico, químico, de dispositivos médicos e de gestão da cadeia de abastecimento tem dificuldade em responder. Estas organizações têm de cumprir requisitos rigorosos de qualidade, segurança e conformidade em cada região geográfica onde os seus produtos são distribuídos. A tendência atual na gestão da conformidade regulamentar está a avançar para uma harmonização global da qualidade e segurança, com ênfase em práticas robustas. Quer seja um fabricante ou um fornecedor, a sua expansão de mercado, melhoria contínua e satisfação do cliente dependem principalmente dos padrões de qualidade do seu negócio. O Centro de Excelência (CoE) de Conformidade Regulamentar, Auditoria e Validação da Freyr pode ajudar neste esforço, prestando-lhe serviços profissionais de Conformidade, Auditoria e Validação para os setores farmacêutico, de dispositivos médicos, de bens de consumo e de cuidados de saúde, tais como cGMP (Boas Práticas de Fabrico Atuais), GCP Boas Práticas Clínicas), GDP Boas Práticas de Distribuição), Boas Práticas de Laboratório (GLP), Boas Práticas de Farmacovigilância GPVP ) eValidação de Sistemas Informáticos GxP (CSV). A nossa equipa de consultoria em conformidade farmacêutica fornece soluções personalizadas para responder aos seus desafios de conformidade específicos.
A Freyr presta serviços de conformidade regulamentar, auditoria e validação que envolvem a avaliação dos seus requisitos e a sugestão de melhorias nos processos empresariais, com o objetivo de garantir a satisfação do cliente. Através da elaboração de relatórios de auditoria de conformidade e das nossas estratégias de preparação, fornecemos relatórios de conformidade e auditoria (análise de lacunas), incluindo sugestões de Ações Corretivas e Preventivas (CAPA) para evitar potenciais observações 483 e conclusões de auditorias de conformidade por parte das entidades reguladoras. A consultoria em conformidade farmacêutica da Freyr estende-se também à consultoria em conformidade de automação farmacêutica, garantindo que os seus sistemas automatizados cumprem as expectativas regulamentares em constante evolução. A nossa abordagem abrangente à gestão da conformidade garante que todas as fases do ciclo de vida do seu processo são monitorizadas e otimizadas para o alinhamento regulamentar.
Prestamos serviços de conformidade regulamentar e validação para garantir que todos os seus processos e produtos estejam em conformidade com os requisitos aplicáveis em matéria de qualidade, segurança da informação e conformidade regulamentar, tais como (entre outros) os seguintes:
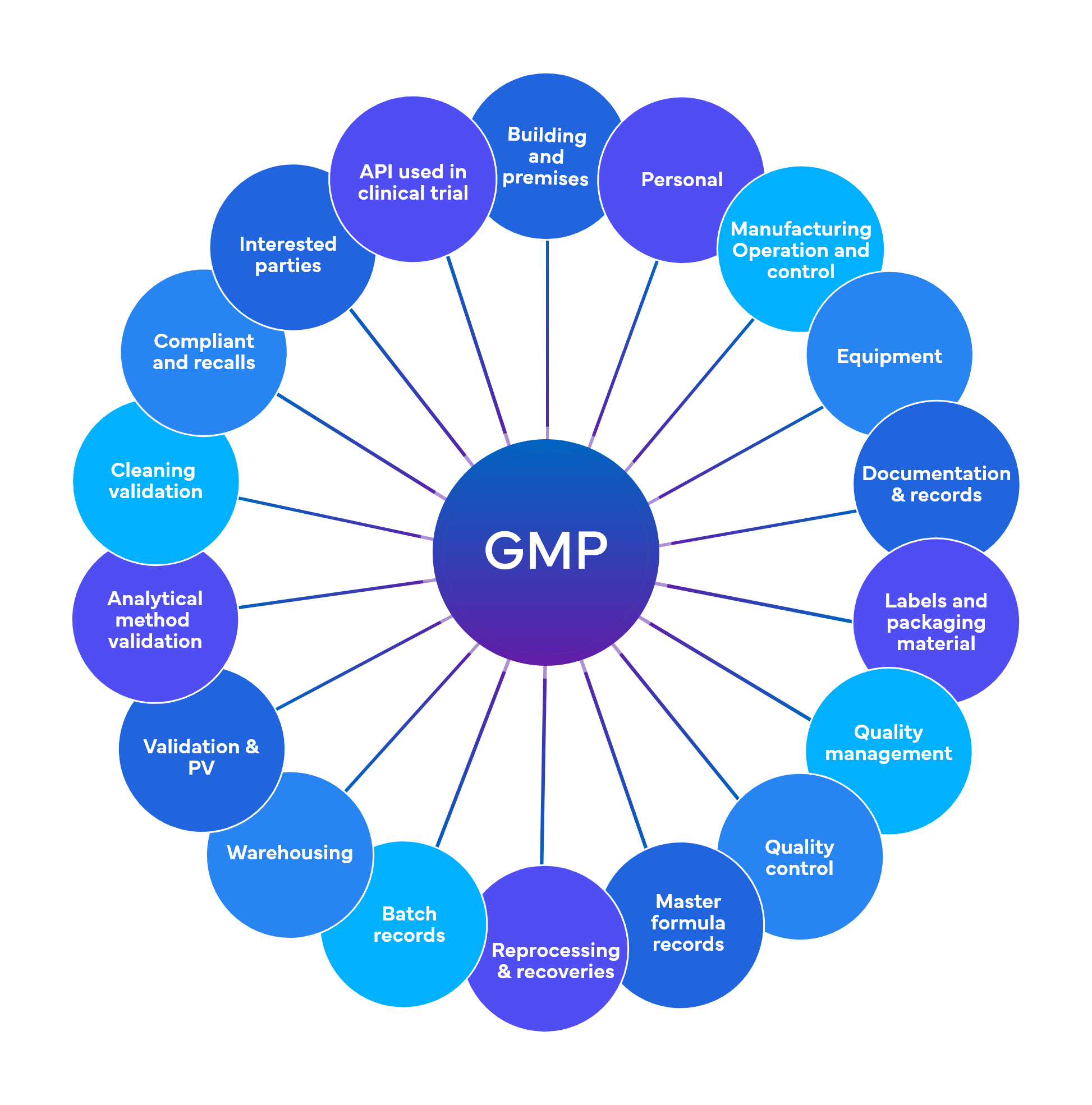
A Freyr realiza cerca de 700 verificações a um nível preliminar, distribuídas por 18-19 áreas funcionais de GMP.
Conformidade, Auditoria e Validação da Freyr
Serviços de Conformidade, Auditoria e Validação
Qualidade e Conformidade Regulamentar – Boas Práticas de Fabrico Atuais (BPFA)
- ISO / IEC 17025: 2017 - Requisitos Gerais para a Competência de Laboratórios de Ensaio e Calibração
- OCDE (Organização para a Cooperação e Desenvolvimento Económico) - Diretrizes de Boas Práticas de Laboratório
- Guia EURACHEM / CITAC: Guia para a Qualidade em Química Analítica - Um Auxílio à Acreditação, 3.ª Edição (2016), deve ser seguido nos procedimentos analíticos
- 21 CFR 58: Boas Práticas de Laboratório para Estudos Laboratoriais Não Clínicos
- Guia para os Regulamentos GLP do REINO UNIDO, Fev. 2000 (pela GLPMA)
- Manual da WHO sobre Boas Práticas de Laboratório (GLP): Práticas de Qualidade para Investigação e Desenvolvimento Não Clínico Regulamentado
- Health Canada: Documento de Orientação Finalizado - Dados de Estudos Laboratoriais Não Clínicos que Suportam Submissões de Produtos Farmacêuticos: Adesão às Boas Práticas de Laboratório
- Normas da OSHA (Occupational Safety and Health Administration)
- Diretrizes ICH Aplicáveis
Boas Práticas de Laboratório.
- ISO / IEC 17025: 2017 - Requisitos Gerais para a Competência de Laboratórios de Ensaio e Calibração
- OCDE (Organização para a Cooperação e Desenvolvimento Económico) - Diretrizes de Boas Práticas de Laboratório
- Guia EURACHEM / CITAC: Guia para a Qualidade em Química Analítica - Um Auxílio à Acreditação, 3.ª Edição (2016), deve ser seguido nos procedimentos analíticos
- 21 CFR 58: Boas Práticas de Laboratório para Estudos Laboratoriais Não Clínicos
- Guia para os Regulamentos GLP do REINO UNIDO, Fev. 2000 (pela GLPMA)
- Manual da WHO sobre Boas Práticas de Laboratório (GLP): Práticas de Qualidade para Investigação e Desenvolvimento Não Clínico Regulamentado
- Health Canada: Documento de Orientação Finalizado - Dados de Estudos Laboratoriais Não Clínicos que Suportam Submissões de Produtos Farmacêuticos: Adesão às Boas Práticas de Laboratório
- Normas da OSHA (Occupational Safety and Health Administration)
- Diretrizes ICH Aplicáveis
Boas Práticas Clínicas (GCP) e Boas Práticas de Farmacovigilância (GVP)
- ICH Diretriz Tripartida Harmonizada: Diretriz para Boas Práticas Clínicas - E6
- Especificação do Relatório Individual de Segurança de Casos (ICSR) E2B(R3) e Ficheiros Relacionados
- Relatório Periódico de Avaliação Benefício-Risco (PBRER) E2C(R2)
- Outras Diretrizes ICH Aplicáveis
- Diretrizes sobre os Módulos das Boas Práticas de Farmacovigilância (GVP).
- Requisitos da FDA para Notificação de Segurança para INDs e Estudos BA/BE
- Relatórios de Segurança Pós-Comercialização para Medicamentos de Uso Humano e Produtos Biológicos, Incluindo Vacinas
- Especificações de Implementação Regional da FDA para Relatórios ICH E2B(R3) ao Sistema de Notificação de Eventos Adversos da FDA (FAERS)
- Fornecer Submissões em Formato Eletrónico – Perguntas e Respostas Técnicas sobre ICSRs Pós-Comercialização Não Acelerados
- Planeamento de Farmacovigilância E2E
Segurança da Informação, Privacidade de Dados e Validação de Sistemas Computorizados (CSV)
- ISO 27001: 2013 Tecnologia da Informação – Técnicas de Segurança – Sistema de Gestão da Segurança da Informação – Requisitos
- ISO 27002: 2013 Tecnologia da Informação – Técnicas de Segurança – Código de Boas Práticas para a Gestão da Segurança da Informação
- USFDA 21 CFR Part 11: Registos Eletrónicos; Assinaturas Eletrónicas – Âmbito e submissão
- Guia BPF da UE Anexo 11
- Notificação da Diretriz Japonesa ERES N.º 0401022
- GAMP 5: Uma Abordagem Baseada no Risco para Sistemas Computorizados GxP em Conformidade
- USFDA – Diretrizes de Validação de Software
- Diretrizes ICH QSEM Aplicáveis
- Planear e criar SOPs e controlar as instalações de fabrico
- Modelo de processo integrado
- Manter a imagem da marca
- Serviços de avaliação de risco
- Poupança geral de custos
- Implementar processos de negócio eficazes e em conformidade
- Estabelecer estratégias de validação e qualificação
- Experiência em conformidade regulamentar e de auditoria
- Auditores de conformidade especializados
A nossa abordagem de consultoria em qualidade e conformidade foi concebida para proporcionar insights práticos e melhorias sustentáveis, apoiando a sua empresa na conquista da excelência operacional e do sucesso em matéria de conformidade regulamentar.



 Serviços de Conformidade e Auditoria
Serviços de Conformidade e Auditoria










