
A gestão de risco é uma atividade crítica em todas as fases do ciclo de vida do dispositivo médico, uma vez que afeta diretamente a segurança e o bem-estar dos pacientes. Os riscos são inevitáveis; no entanto, podem ser mitigados se as empresas estiverem cientes dos perigos iminentes e seguirem procedimentos eficazes de gestão de risco.
A Análise de Modos de Falha e Efeitos (FMEA) é uma ferramenta de revisão para identificar possíveis falhas num projeto, num processo de fabrico ou montagem, ou num produto ou serviço num dispositivo. “Modos de falha” refere-se às formas como um dispositivo pode falhar, o que pode potencialmente afetar os pacientes. “Análise de efeitos” refere-se ao exame das consequências dessas falhas. É uma abordagem passo a passo para garantir a fiabilidade e qualidade de um dispositivo.
Existem dois tipos de FMEAs: FMEA de Design (DFMEA) e FMEA de Processo (PFMEA). No contexto dos dispositivos médicos, os fabricantes de dispositivos utilizam o DFMEA para avaliar falhas relacionadas com o design e as especificações do dispositivo, enquanto o PFMEA é utilizado para melhorar o processo de fabrico.
Embora a FMEA envolva o aspeto do risco, não é um sistema de gestão de riscos. Os requisitos de gestão de riscos são definidos pela ISO 14971:2019, que serve como um quadro para os fabricantes de dispositivos médicos preverem a probabilidade de riscos e as suas consequências ao longo do ciclo de vida do produto. A metodologia de avaliação de riscos da FMEA não está alinhada com a ISO 14971:2019. A FMEA tem a sua própria norma internacionalmente aceite, a IEC 60812:2018, que explica como a análise de modos de falha e efeitos é planeada, realizada, documentada e mantida. A FMEA e a ISO 14971 diferem uma da outra em certos aspetos, que são os seguintes:
Utilização Normal e Condição de Falha
De acordo com a ISO 14971, a gestão de riscos inclui tanto a utilização normal como a incorreta do dispositivo, enquanto a FMEA inclui riscos associados apenas à falha do dispositivo. Um exemplo simples seria os riscos associados à linha intravenosa (IV). A ISO 14971 considera o risco potencial de infeção, apesar da administração correta de um IV. Pode ser devido a várias razões, como baixa imunidade do paciente e infeções presentes no ambiente hospitalar/clínico. Estes riscos não são tidos em conta numa avaliação FMEA. Embora os fabricantes de dispositivos médicos não possam evitar totalmente estes riscos, podem informar os utilizadores sobre os riscos residuais associados à utilização do dispositivo.
Avaliação da Gravidade
A ISO 14971 considera a gravidade do risco com base nos danos à vida das pessoas, enquanto a FMEA considera o mesmo com base em falhas no desempenho do sistema. A gravidade do risco pode ser considerada baixa na FMEA se houver uma perda menor de função, mesmo que possa levar à perda de vidas. A gravidade será considerada alta se o dispositivo avariar.
Por exemplo, a FDA recolheu um fio-guia (Classe I) destinado a ser inserido num cateter percutâneo para direcionar o cateter através de um vaso sanguíneo. O fio-guia em questão tem o potencial de o revestimento se soltar. A FMEA classificou potencialmente isto como uma gravidade de baixo risco pós-avaliação, mas pode ter implicações graves na saúde do paciente.
O Procedimento de Avaliação de Risco / Modos de Falha
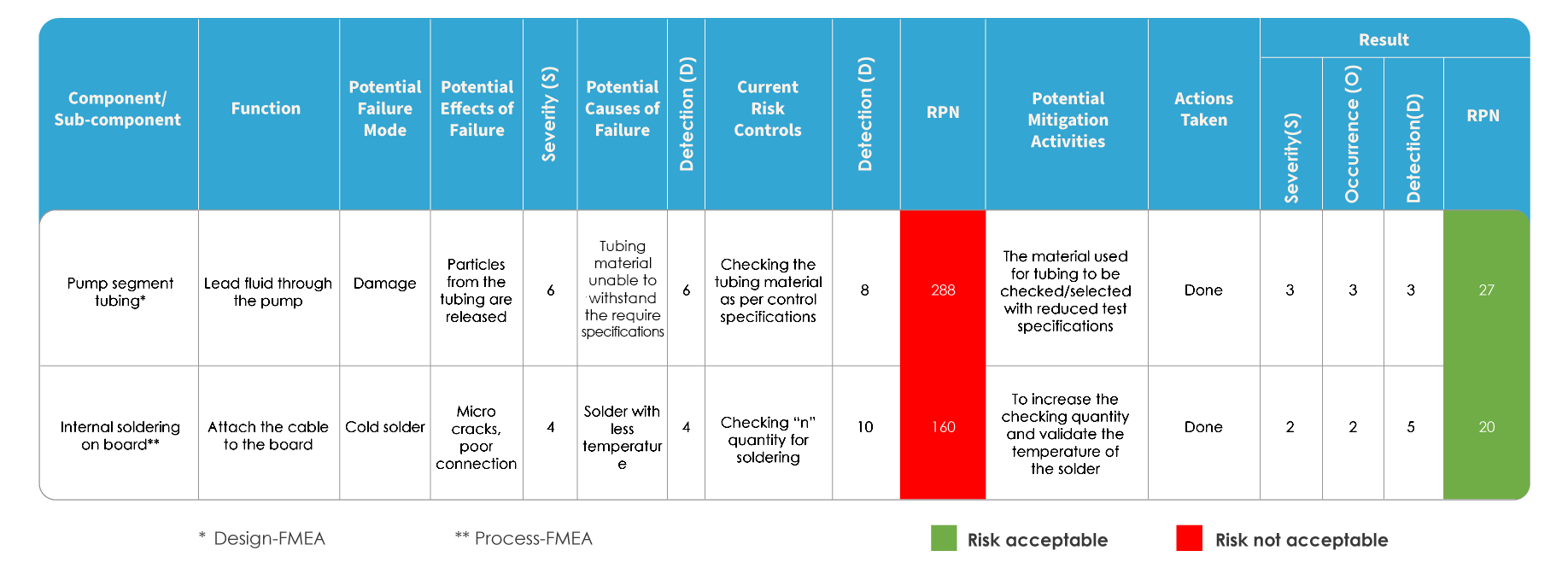
A FMEA e a ISO 14971 diferem na forma como o risco é avaliado. Na FMEA, o risco é avaliado através da identificação de potenciais modos e efeitos de falha, seguida da classificação da gravidade das falhas. Cada uma das causas potenciais é identificada e a probabilidade de ocorrência é determinada. O risco é avaliado com base no Número de Prioridade de Risco (NPR).
Mapeamento FMEA
No caso do mapeamento da gestão de riscos de acordo com a ISO 14971, é utilizada uma ferramenta de rastreabilidade conhecida como Matriz de Rastreabilidade de Perigos (HTM). Inclui a análise, avaliação, controlo e avaliação do risco residual.
Matriz de Rastreabilidade de Perigos
| Análise de Risco | Risco Aval. | Controlo de Risco | ||||||||||||
| Identificação | Perigo | Sequência ou Combinação de Eventos Razoavelmente Previsível | Perigoso Situação | Dano | Ocorrência | Gravidade | Aceitável? | Opções e Fundamentação do Controlo de Risco | Controlo de Risco Medidas | Risco Controlo Verificação | Estado | Potencial de Risco | Gravidade do Risco | Risco Residual |
| 1 | Tensão de linha | O utilizador usa o dispositivo | O utilizador/paciente pode ser exposto à tensão da rede enquanto em contacto com o dispositivo | Morte do Utilizador / Doente | 5 | 5 | N | A segurança pode ser assegurada através de uma alteração no design e de medidas de proteção. | Conceção de acordo com a IEC 61010. | Os testes elétricos devem ser realizados de acordo com a IEC 61010. | Concluído | 2 | 2 | Y |
![]()
Após discutir as diferenças entre os dois, pode-se concluir que a ISO 14971 segue uma abordagem abrangente à gestão de riscos, enquanto a FMEA é mais uma ferramenta de fiabilidade. No entanto, os fabricantes de dispositivos médicos teriam de cumprir a ISO 14971 para satisfazer as expectativas das autoridades de regulamentação relativamente às normas de gestão de riscos.
Para saber mais sobre os serviços de consultoria em conformidade com a ISO 14971:2016 e gestão de riscos, contacte a Freyr hoje!









